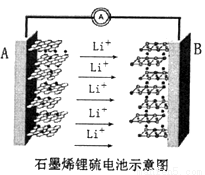
��Ŀ����
���ۡ�ͭ�ۻ������Ʒ11.6g������2.0 mol/L����������Һ����ַ�Ӧ��ʣ��������������������Һ����仯���±���
������Һ/mL | 20.0 | 40.0 | 60.0 | 80.0 |
ʣ�����/g | 9.36 | 7.12 | 4.88 | 3.20 |
��ش�
(1)��Ʒ������ͭ�����ʵ���֮��n(Fe����n(Cu)=________ ��
(2)�ڷ�Ӧ�����ϵ�У��ټ���4.0mol/L��H2O2��Һ25.0mL������������������Һ����ַ�Ӧ����Һ�д��ڵĸ��������ӵ����ʵ����ֱ��Ƕ��٣�__________________
̼���仯���������ǵ��ճ������ũҵ��������ѧ�о���������Ҫ�����á��ش������й����⣺
(1)ú̿������������Ϊ�㷺��ȼ�ϣ�����ú̿��������´�����Ⱦ����ȼú�����е�SO2�ɲ���̼��ƽ�Һ�����գ�����ȼú�����Ϳ���ͬʱ���뵽��CaCO3�Ľ�Һ�У�ʹSO2�����ա��ٸ÷�Ӧ����ʯ��(CaSO4 •2H2O)����ѧ����ʽΪ____________________��
�ڱ�״���£�ij��������SO2����Ϊ2.1��10-3g •L-1����Ӧ��ת��3 mol����ʱ��������
״�������������Ϊ___________L��������λ��Ч���֣���
(2)��ҵ�����Ļ���ԭ����:�ڸ����£���̿ȼ�����ɵ�CO������ʯ�����������ﻹԭ�õ�����
��֪��
��Fe2O3(s)+3C(s,ʯī)==2Fe(s)+3CO(g) ��H= +489.0 kJ• mol-1��
��C(s,ʯī)+CO2(g) ==2CO(g) ��H= +172.5 kJ• mol-1��
��CO��ԭFe2O3(s)���Ȼ�ѧ����ʽΪ_______________________��
(3)̼�������(DMC)��һ�����������������졢��;�㷺�Ļ���ԭ�ϡ�һ���¶�ʱ�����ݻ�Ϊ1.0 L�ĺ����ܱ������г���2.5molCH3OH(g)������CO2��5��10-3�����������з�����Ӧ��2CH3OH(g) +CO2(g)  CH3OCOOCH3(g) +H2O(g) ��H= -15.5kJ• mol-1���״�ת����(TON)�뷴Ӧʱ��Ĺ�ϵ��ͼ1��ʾ��
CH3OCOOCH3(g) +H2O(g) ��H= -15.5kJ• mol-1���״�ת����(TON)�뷴Ӧʱ��Ĺ�ϵ��ͼ1��ʾ��
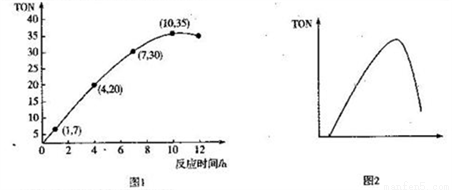
��֪:TON=
�ٸ��¶�ʱ���״������ת����Ϊ_______________��
�� 0 ~7 h��DMC��ƽ����Ӧ������_______mol��L-1��h-1��������λ��Ч���֣���
��ͼ2�Ǽ״�ת������ij���������ı仯���ߣ���������������_______��Ϊʹ�÷�Ӧ����
��Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��______________________��(���һ������)��
(4)CO2�ܽ���ˮ�γ�̼�ᡣ̼���������ĵ��볣�����±���ʾ��
���� | ̼�� | ������ |
���볣��(Ka) | Ka1=4.4��l0-7 Ka2=5.6��10-11 | 3.0��10-8 |
��NaClO��Һ��ͨ������CO2 ����Ӧ�����ӷ���ʽΪ_____________________��0.03 mol • L-1 NaClO ��Һ�� pH=________________��
����þ����(MgSO4��7H2O)��һ����Ҫ�Ļ���ԭ�ϣ��������Ƹըҩ����ֽ�������ȡ�����þ��(��Ҫ�ɷ���̼��þ��������FeCO3�Ͳ���������)Ϊԭ����ȡ����þ������������£�

��֪������������������������ʽ����ʱ��Һ��pH���±���
������ | Mg2�� | Fe2�� | Fe3�� |
��ʼ���� | 9.1 | 7.6 | 1.9 |
��ȫ���� | 11.1 | 9.7 | 3.2 |
(1) �������������У�����H2O2��Һ��Ŀ����________(�����ӷ���ʽ��ʾ)���������������У��ð�ˮ����pH�ķ�Χ��________��
(2) �����ˡ�������Һ�к��е�������ΪMg2����________��
(3) ���ᾧ��������������Ũ����Һ��ʹ�õ�ʵ������������̨(����Ȧ)���ƾ��ơ���������____________________����
(4) �ⶨ����þ������Ʒ��MgSO4��7H2O�ĺ�������������ʵ�鷽����
��. ��ȡ��������þ������Ʒ1.500 g���������EDTA�����100 mL pH��9��10֮�����ҺA��
��. ��ȡ25.00 mL��ҺA����ƿ�У���0.1000 mol��L��1 Zn2������Һ�������EDTA��Ӧ������Zn2������Һ20.00 mL��
��. ����ȡ25.00 mL��ҺA����һֻ��ƿ�У�����pHΪ5��6����0.100 0 mol��L��1 Zn2������Һ��֮��ַ�Ӧ������Zn2������Һ35.00 mL��
��֪����pHΪ9��10ʱ��Mg2����Zn2��������EDTA(H2Y2��)��Ӧ��Mg2����H2Y2��===MgH2Y����Zn2����H2Y2��===ZnH2Y
��pHΪ5��6ʱ��Zn2������EDTA��Ӧ��������MgH2Y��Ӧ��Zn2����MgH2Y===ZnH2Y��Mg2��
����Ʒ�����ʲ����뷴Ӧ��
��������þ������Ʒ��MgSO4��7H2O����������________��(д���������)��