题目内容
常温下,对pH=10的NaHCO3溶液中,各微粒的物质的量浓度分析正确的是
| A.c(CO32-)>c(H2CO3) |
| B.c(Na+)>c(HCO3-)>c(H+)>c(OH-) |
| C.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
D
试题分析:HCO3-水解生成H2CO3和OH-,HCO3-电离生成CO32-和H+,由于pH=10,说明水解程度大于电离,A选项不正确,pH=10的NaHCO3溶液显碱性,c(OH-) >c(H+),B选项不正确,根据电荷守恒式,应为c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),C选项不正确,由物料守恒式,n(Na):n(C)=1:1,。D选项正确,。

练习册系列答案
相关题目
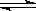 H3O++CO32-
H3O++CO32-
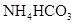


 CH3COO- + H3O+
CH3COO- + H3O+