题目内容
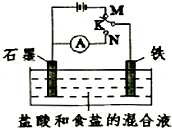 (2013?日照二模)用如图所示装置进行实验,下列叙述不正确的是( )
(2013?日照二模)用如图所示装置进行实验,下列叙述不正确的是( )分析:K与N连接时,形成原电池,为析氢腐蚀的模型,铁被腐蚀,石墨电极产生H2;
K与M连接时,构成电解池,石墨为阳极,初始阶段石墨电极的反应为:2Cl--2e-=Cl2↑,Cl-放电完毕,OH-再放电,电极反应为4OH--4e-═2H2O+O2↑,铁为阴极,铁电极的反应为:2H++2e-=H2↑,氢离子浓度减小,溶液的pH增大.
K与M连接时,构成电解池,石墨为阳极,初始阶段石墨电极的反应为:2Cl--2e-=Cl2↑,Cl-放电完毕,OH-再放电,电极反应为4OH--4e-═2H2O+O2↑,铁为阴极,铁电极的反应为:2H++2e-=H2↑,氢离子浓度减小,溶液的pH增大.
解答:解:A.K与N连接时,形成原电池,为析氢腐蚀的模型,铁被腐蚀,故A正确;
B.K与N连接时,形成原电池,为析氢腐蚀的模型,铁被腐蚀,石墨电极反应式为2H++2e-=H2↑,产生H2,故B正确;
C.K与M连接时,构成电解池,铁电极的反应为:2H++2e-=H2↑,氢离子浓度减小,溶液的pH增大,故C正确;
D.K与M连接时,构成电解池,石墨为阳极,初始阶段石墨电极的反应为:2Cl--2e-=Cl2↑,故D错误;
故选D.
B.K与N连接时,形成原电池,为析氢腐蚀的模型,铁被腐蚀,石墨电极反应式为2H++2e-=H2↑,产生H2,故B正确;
C.K与M连接时,构成电解池,铁电极的反应为:2H++2e-=H2↑,氢离子浓度减小,溶液的pH增大,故C正确;
D.K与M连接时,构成电解池,石墨为阳极,初始阶段石墨电极的反应为:2Cl--2e-=Cl2↑,故D错误;
故选D.
点评:本题考查原电池与电解原理,难度不大,电化学的有关知识一直是高考考查的重点,原电池与电解池的本质都是氧化还原反应,注意掌握电解池中离子放电顺序.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
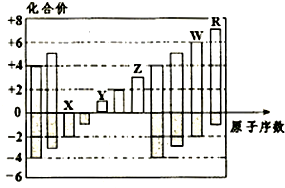 (2013?日照二模)如图所示是五种短周期元素化合价与原子序数的关系,下列说法不正确的是( )
(2013?日照二模)如图所示是五种短周期元素化合价与原子序数的关系,下列说法不正确的是( )