题目内容
12.8g铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为4.48L.铜和硝酸反应的化学方程式为:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
试计算:
(1)被还原的硝酸的物质的量
(2)4.48L气体中各成分的物质的量.
解:(1)设气体的平均分子式为NOx,被还原的硝酸的物质的量为y,
标准状况下生成气体的物质的量为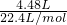 =0.2mol,气体分子与被还原的硝酸的关系式为
=0.2mol,气体分子与被还原的硝酸的关系式为
HNO3--NOx
1 1
ymol 0.2mol
y=0.2mol,
答:被还原的硝酸的物质的量为0.2mol;
(2)铜与硝酸反应中,铜失电子作还原剂,硝酸得电子作氧化剂,在氧化还原反应中得失电子数相等,利用电子守恒,列方程组,得出NO、NO2的物质的量.
铜的物质的量为 =0.2mol,则0.2molCu变成Cu2+失去的电子为0.2mol×2=0.4mol,
=0.2mol,则0.2molCu变成Cu2+失去的电子为0.2mol×2=0.4mol,
设生成NO的物质的量为mmol,NO2的物质的量为nmol,混合气体的物质的量为0.2mol,即
m+n=0.2
由氧化还原反应中得失电子数相等得;
3m+n=0.4
列方程组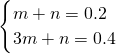 ,解得m=0.1mol,n=0.1mol,
,解得m=0.1mol,n=0.1mol,
答:4.48L气体中NO为0.1mol,NO2的物质的量为0.1mol.
分析:(1)铜与硝酸反应生成的气体无论是NO还是NO2,一个气体分子中含有一个N原子,一个硝酸分子中含有一个N原子,根据原子守恒,气体的物质的量与被还原的硝酸的物质的量相等.
(2)铜与硝酸反应中,铜失电子作还原剂,硝酸得电子作氧化剂,在氧化还原反应中得失电子数相等,利用电子守恒,列方程组,得出NO、NO2的物质的量.
点评:本题考查的是硝酸的性质及结合方程式的计算,巧妙利用守恒法、关系式进行计算,有事半功倍之效.估算法、差量法、平均值法等都是做题时常用的方法.
标准状况下生成气体的物质的量为
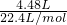 =0.2mol,气体分子与被还原的硝酸的关系式为
=0.2mol,气体分子与被还原的硝酸的关系式为HNO3--NOx
1 1
ymol 0.2mol
y=0.2mol,
答:被还原的硝酸的物质的量为0.2mol;
(2)铜与硝酸反应中,铜失电子作还原剂,硝酸得电子作氧化剂,在氧化还原反应中得失电子数相等,利用电子守恒,列方程组,得出NO、NO2的物质的量.
铜的物质的量为
 =0.2mol,则0.2molCu变成Cu2+失去的电子为0.2mol×2=0.4mol,
=0.2mol,则0.2molCu变成Cu2+失去的电子为0.2mol×2=0.4mol,设生成NO的物质的量为mmol,NO2的物质的量为nmol,混合气体的物质的量为0.2mol,即
m+n=0.2
由氧化还原反应中得失电子数相等得;
3m+n=0.4
列方程组
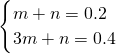 ,解得m=0.1mol,n=0.1mol,
,解得m=0.1mol,n=0.1mol,答:4.48L气体中NO为0.1mol,NO2的物质的量为0.1mol.
分析:(1)铜与硝酸反应生成的气体无论是NO还是NO2,一个气体分子中含有一个N原子,一个硝酸分子中含有一个N原子,根据原子守恒,气体的物质的量与被还原的硝酸的物质的量相等.
(2)铜与硝酸反应中,铜失电子作还原剂,硝酸得电子作氧化剂,在氧化还原反应中得失电子数相等,利用电子守恒,列方程组,得出NO、NO2的物质的量.
点评:本题考查的是硝酸的性质及结合方程式的计算,巧妙利用守恒法、关系式进行计算,有事半功倍之效.估算法、差量法、平均值法等都是做题时常用的方法.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目