题目内容
一次性筷子、一次性饭盒的安全受到社会的关注.专家介绍说,正规的一次性筷子所用的
原料都是质地较好的木材,不用特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为筷子看上去
白一些,他们常用硫磺进行熏蒸漂白,结果造成二氧化硫严重超标,同时硫磺中含铅、汞等重金属,也会
对人体造成铅中毒或汞中毒.
(1)“硫磺熏蒸”是应用二氧化硫的漂白性质,写出硫磺燃烧的化学方程式
(2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量.为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是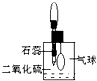 生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
(3)在制一次性筷子时有“抛光”程序:加入滑石粉和木签一起搅拌,起到干燥、打磨的作用,使筷子变得光滑,以免毛疵划人的口腔.已知滑石粉是一种含水的具有层状结构的硅酸盐矿物.其质量组成为MgO 31.88%,SiO263.37%,H2O 4.75%,其化学式为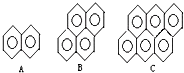
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒.有如右的一系列物质,则A的分子式为
原料都是质地较好的木材,不用特殊加工.但是很多小作坊为了降低成本,使用劣质木材,为筷子看上去
白一些,他们常用硫磺进行熏蒸漂白,结果造成二氧化硫严重超标,同时硫磺中含铅、汞等重金属,也会
对人体造成铅中毒或汞中毒.
(1)“硫磺熏蒸”是应用二氧化硫的漂白性质,写出硫磺燃烧的化学方程式
S+O2
SO2
| ||
S+O2
SO2
| ||
(2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量.为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是
紫色石蕊试液变红、气球鼓胀起来
紫色石蕊试液变红、气球鼓胀起来
;为比较SO2 和CO2溶解性的大小,某学生采取同样的装置和操作,能说明SO2在水中的溶解性大于CO2在水中溶解性的实验现象是SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度
SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度
.某学 生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为
生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色)
品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色)
,接着向溶液中加入足量氯水,实验现象为 先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液)
先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液)
,再滴加BaCl2溶液,实验现象为生成白色沉淀(BaSO4)
生成白色沉淀(BaSO4)
.(3)在制一次性筷子时有“抛光”程序:加入滑石粉和木签一起搅拌,起到干燥、打磨的作用,使筷子变得光滑,以免毛疵划人的口腔.已知滑石粉是一种含水的具有层状结构的硅酸盐矿物.其质量组成为MgO 31.88%,SiO263.37%,H2O 4.75%,其化学式为
Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O
Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O
.
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒.有如右的一系列物质,则A的分子式为
C10H8
C10H8
,A、B、C可以互称同系物吗?为什么?不能
不能
因为A、B、C相差n个C6H2,不是n个CH2
因为A、B、C相差n个C6H2,不是n个CH2
.该系列化合物里碳的最大质量分数为97.3%
97.3%
;若E是A的一个氢原子被羟基取代的产物,预测E可能具有哪些化学性质(至少举2条)E能与溴水发生取代反应、
E能与溴水发生取代反应、
E与FeCl3能发生显色反应、E能和碳酸钠溶液反应
E与FeCl3能发生显色反应、E能和碳酸钠溶液反应
.分析:(1)硫燃烧生成二氧化硫;
(2)二氧化硫极易溶于水,水溶液呈酸性,二氧化碳微溶于水,可根据气球的鼓胀程度比较二者的溶解性,二氧化硫具有漂白性,能使品红褪色,滴加氯水时发生氧化还原反应生成硫酸,滴加BaCl2溶液,生成硫酸钡沉淀;
(3)根据质量分数计算物质的量比值,注意硅酸盐的书写顺序为:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水;
(4)因该系列化合物的通式为C6n+4H2n+6(n≥1),用数学极限思想求得C%的最大值为97.3%.根据题意知E是C10H7-OH,应具有与苯酚相似的化学性质,可推测E能与溴水发生取代反应、E与FeCl3能发生显色反应、E能和碳酸钠溶液反应等.
(2)二氧化硫极易溶于水,水溶液呈酸性,二氧化碳微溶于水,可根据气球的鼓胀程度比较二者的溶解性,二氧化硫具有漂白性,能使品红褪色,滴加氯水时发生氧化还原反应生成硫酸,滴加BaCl2溶液,生成硫酸钡沉淀;
(3)根据质量分数计算物质的量比值,注意硅酸盐的书写顺序为:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水;
(4)因该系列化合物的通式为C6n+4H2n+6(n≥1),用数学极限思想求得C%的最大值为97.3%.根据题意知E是C10H7-OH,应具有与苯酚相似的化学性质,可推测E能与溴水发生取代反应、E与FeCl3能发生显色反应、E能和碳酸钠溶液反应等.
解答:解:(1)硫燃烧生成二氧化硫,反应为S+O2
SO2,故答案为:S+O2
SO2;
(2)二氧化硫极易溶于水,水溶液呈酸性,生成H2SO3,二氧化碳微溶于水,可根据气球的鼓胀程度比较二者的溶解性,二氧化硫具有漂白性,能使品红褪色,滴加氯水时发生反应SO2+Cl2+2H2O═H2SO4+2HCl,先变红后褪色,再滴加BaCl2溶液,生成硫酸钡沉淀,故答案为:紫色石蕊试液变红、气球鼓胀起来;SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度;
品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色);先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液); 生成白色沉淀(BaSO4);
(3)根据质量分数计算物质的量比值,注意硅酸盐的书写顺序为:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,
根据MgO 31.88%,SiO263.37%,H2O 4.75%,则有:n(MgO):n(SiO2):n(H2O )=
:
:
=3:4:1,所以化学式为Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O,
故答案为:Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O;
(4)因该系列化合物的通式为C6n+4H2n+6(n≥1),用数学极限思想求得C%的最大值为97.3%.根据题意知E是C10H7-OH,应具有与苯酚相似的化学性质,可推测E能与溴水发生取代反应、E与FeCl3能发生显色反应、E能和碳酸钠溶液反应等.
故答案为:C10H8;不能;因为A、B、C 相差n个C6H2,不是n个CH2; 97.3%;E能与溴水发生取代反应、E与FeCl3能发生显色反应、E能和碳酸钠溶液反应;
| ||
| ||
(2)二氧化硫极易溶于水,水溶液呈酸性,生成H2SO3,二氧化碳微溶于水,可根据气球的鼓胀程度比较二者的溶解性,二氧化硫具有漂白性,能使品红褪色,滴加氯水时发生反应SO2+Cl2+2H2O═H2SO4+2HCl,先变红后褪色,再滴加BaCl2溶液,生成硫酸钡沉淀,故答案为:紫色石蕊试液变红、气球鼓胀起来;SO2溶解时气球鼓胀的程度大于CO2溶解时气球的鼓胀程度;
品红溶液的红色褪去(品红、SO2结合成不稳定的化合物),溶液显浅紫色(石蕊的颜色);先变红后褪色(足量氯水能氧化SO2、石蕊和品红试液); 生成白色沉淀(BaSO4);
(3)根据质量分数计算物质的量比值,注意硅酸盐的书写顺序为:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,
根据MgO 31.88%,SiO263.37%,H2O 4.75%,则有:n(MgO):n(SiO2):n(H2O )=
| 31.88 |
| 40 |
| 63.37 |
| 60 |
| 4.75 |
| 18 |
故答案为:Mg3(Si4O10)(OH)2或3MgO?4SiO2?H2O;
(4)因该系列化合物的通式为C6n+4H2n+6(n≥1),用数学极限思想求得C%的最大值为97.3%.根据题意知E是C10H7-OH,应具有与苯酚相似的化学性质,可推测E能与溴水发生取代反应、E与FeCl3能发生显色反应、E能和碳酸钠溶液反应等.
故答案为:C10H8;不能;因为A、B、C 相差n个C6H2,不是n个CH2; 97.3%;E能与溴水发生取代反应、E与FeCl3能发生显色反应、E能和碳酸钠溶液反应;
点评:本题考查较为综合,涉及二氧化硫的性质以及硅酸盐的组成、有机物的性质等,本题难度较大,做题时注意把握基础知识的积累,本题易错点为(2)题,注意实验原理的探究和比较.

练习册系列答案
相关题目
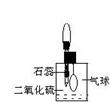 (2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量。为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是________。为比较SO2 和CO2溶解性的大小,某学生采取同样的装置和操作,能说明SO2在水中的溶解性大于CO2在水中溶解性的实验现象是____________。某学生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为_______,接着向溶液中加入足量氯水,实验现象为_______,再滴加BaCl2溶液,实验现象为_____________。
(2)防止、减小毒筷“中毒”最简单的方法是用凉水清洗筷子表面,减少二氧化硫的含量。为研究SO2的溶解性质,某学生做如下实验:如右图,集气瓶中收集的是SO2,瓶塞系着瘪气球,向瓶中滴加紫色石蕊试液,实验现象是________。为比较SO2 和CO2溶解性的大小,某学生采取同样的装置和操作,能说明SO2在水中的溶解性大于CO2在水中溶解性的实验现象是____________。某学生取出瓶中溶液,将其滴入品红溶液,充分振荡,实验现象为_______,接着向溶液中加入足量氯水,实验现象为_______,再滴加BaCl2溶液,实验现象为_____________。 (4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒。有如右的一系列物质,则A的分子式为 ,A、B、C 可以互称同系物吗?为什么?_____________?该系列化合物里碳的最大质量分数为 ? 若E是A的一个氢原子被羟基取代的产物,预测E可能具有哪些化学性质(至少举2条)
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒。有如右的一系列物质,则A的分子式为 ,A、B、C 可以互称同系物吗?为什么?_____________?该系列化合物里碳的最大质量分数为 ? 若E是A的一个氢原子被羟基取代的产物,预测E可能具有哪些化学性质(至少举2条) 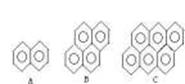 (4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒。有如右的一系列物质,则A的分子式为 ,A、B、C 可以互称同系物吗?为什么?_____________?该系列化合物里碳的最大质量分数为 ? 若E是A的一个氢原子被羟基取代的产物,预测E可能具有哪些化学性质(至少举2条)
(4)有的厂家用石蜡代替“滑石粉抛光”,石蜡是含碳原子数(C20~C30)较多的稠环芳香烃,常温下为固体,温度高时熔化后可随食物进入人体致使慢性中毒。有如右的一系列物质,则A的分子式为 ,A、B、C 可以互称同系物吗?为什么?_____________?该系列化合物里碳的最大质量分数为 ? 若E是A的一个氢原子被羟基取代的产物,预测E可能具有哪些化学性质(至少举2条)