题目内容
(2013?武汉模拟)金属钛呈银白色,因它坚硬.强度大.耐热.密度小,被称为高技术金属.目前生产钛采用氯化法,主要步骤如下:
Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C
2TiCl4+2FeCl3+6CO
TiO2+2Cl2+2C
TiCl4+2CO
Ⅱ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg
Ti+2MgCl2
Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭.
请回答下列问题:
(1)基态钛原子的价电子排布式为
(2)与CO互为等电子体的离子为
(3)在CH2Cl2.HCHO.CO2.C2H4中,碳原子采取sp2杂化的分子有
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟.则TiCl4属于
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是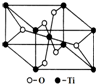
(6)在自然界中TiO2有金红石.板钛矿.锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为
Ⅰ.即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C
| ||
TiO2+2Cl2+2C
| ||
Ⅱ.将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg
| ||
Ⅲ.用稀盐酸溶解MgCl2和过量Mg后得海绵状钛,再在真空熔化铸成钛锭.
请回答下列问题:
(1)基态钛原子的价电子排布式为
3d24s2
3d24s2
.(2)与CO互为等电子体的离子为
CN-(或NO+.C22-)
CN-(或NO+.C22-)
(填化学式).(3)在CH2Cl2.HCHO.CO2.C2H4中,碳原子采取sp2杂化的分子有
HCHO、C2H4
HCHO、C2H4
.(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟.则TiCl4属于
分子
分子
(填“原子”.“分子”或“离子”)晶体.(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是
产生白色沉淀
产生白色沉淀
;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为[Co(NH3)5SO4]Br
[Co(NH3)5SO4]Br
.
(6)在自然界中TiO2有金红石.板钛矿.锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为
6
6
.分析:(1)根据构造原理,由原子序数即可写出基态原子的电子排布式,进而可写出价电子排布式;
(2)根据等电子体的概念写出符合题目要求的等电子体;
(3)可根据分子的构型来判断碳的杂化方式,四面体形属于sp3杂化,平面形中的碳属于sp2杂化,直线形中的碳属于sp杂化;
(4)根据题目中提供的物理性质来判断晶体类型;
(5)络合物由內界和外界组成,络合物溶于水发生电离生成內界离子(络离子)和外界离子,与BaCl2或AgNO3溶液反应的离子肯定为外界离子,由此可判断络合物的组成;
(6)观察晶胞,数数Ti周围距离最近的O的个数即为Ti的配位数.
(2)根据等电子体的概念写出符合题目要求的等电子体;
(3)可根据分子的构型来判断碳的杂化方式,四面体形属于sp3杂化,平面形中的碳属于sp2杂化,直线形中的碳属于sp杂化;
(4)根据题目中提供的物理性质来判断晶体类型;
(5)络合物由內界和外界组成,络合物溶于水发生电离生成內界离子(络离子)和外界离子,与BaCl2或AgNO3溶液反应的离子肯定为外界离子,由此可判断络合物的组成;
(6)观察晶胞,数数Ti周围距离最近的O的个数即为Ti的配位数.
解答:解:(1)钛为22号元素,基态电子排布式为:[Ar]3d24s2,则基态钛原子的价电子排布式为3d24s2,故答案为:3d24s2;
(2)CO为双原子分子,价电子总数为10,则CO的等电子体为离子的为:CN-(或NO+.C22-),故答案为:CN-(或NO+.C22-);
(3)在CH2Cl2.HCHO.CO2.C2H4中,分子构型分别为四面体形、平面三角形、直线形、平面形,所以碳原子的杂化方式分别为sp3、sp2、sp、sp2杂化,
采取sp2杂化的分子有HCHO、C2H4,故答案为:HCHO、C2H4;
(4)因TiCl4在常温下是无色液体,说明熔点低,在水或潮湿空气中易水解而冒白烟,说明钛离子为弱碱阳离子,由此可判断 TiCl4是由共价键结合的分子,晶体类型属于分子晶体.故答案为:分子;
(5)由[Co(NH3)5Br]SO4可知,硫酸根离子为配合物的外界,在水溶液中以离子形式存在,所以会与钡离子结合成白色沉淀.加入BaCl2溶液时,无明显现象,说明硫酸根离子在内界,若加入AgNO3溶液时,产生淡黄色沉淀,说明溴离子在外界,因此另一配合物的化学式为[Co (NH3)5SO4]Br.
故答案为:产生白色沉淀;[Co (NH3)5SO4]Br;
(6)观察晶胞结构,可知每个钛周围距离最近的氧原子有6个,即钛的配位数为6,故答案为:6.
(2)CO为双原子分子,价电子总数为10,则CO的等电子体为离子的为:CN-(或NO+.C22-),故答案为:CN-(或NO+.C22-);
(3)在CH2Cl2.HCHO.CO2.C2H4中,分子构型分别为四面体形、平面三角形、直线形、平面形,所以碳原子的杂化方式分别为sp3、sp2、sp、sp2杂化,
采取sp2杂化的分子有HCHO、C2H4,故答案为:HCHO、C2H4;
(4)因TiCl4在常温下是无色液体,说明熔点低,在水或潮湿空气中易水解而冒白烟,说明钛离子为弱碱阳离子,由此可判断 TiCl4是由共价键结合的分子,晶体类型属于分子晶体.故答案为:分子;
(5)由[Co(NH3)5Br]SO4可知,硫酸根离子为配合物的外界,在水溶液中以离子形式存在,所以会与钡离子结合成白色沉淀.加入BaCl2溶液时,无明显现象,说明硫酸根离子在内界,若加入AgNO3溶液时,产生淡黄色沉淀,说明溴离子在外界,因此另一配合物的化学式为[Co (NH3)5SO4]Br.
故答案为:产生白色沉淀;[Co (NH3)5SO4]Br;
(6)观察晶胞结构,可知每个钛周围距离最近的氧原子有6个,即钛的配位数为6,故答案为:6.
点评:本题考查了电子排布式的书写、等电子体原理、杂化类型的判断、配合物的组成及性质、晶体类型的判断及晶体结构等知识.这些都是高考的热点,是物质结构和性质的核心,应熟练掌握.本题易错点是没注意题目要求,如价电子排布式写成了基态原子的电子排布式,等电子体要求写离子,容易把分子也写上.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
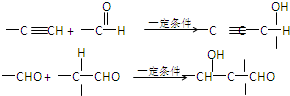



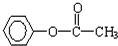 、
、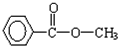 等
等