题目内容
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为_________________________。
(2)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图:
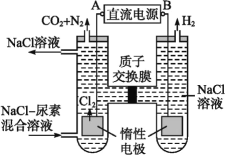
①电源的负极为________(填“A”或“B”)。
②阳极室中发生的反应依次为__________________________、____________________________。
③电解结束后,阴极室溶液的pH与电解前相比将________;若两极共收集到气体13.44 L(标准状况),则除去的尿素为________g(忽略气体的溶解)。
【答案】2NH3+CO2![]() CO(NH2)2+H2O B 2Cl--2e-═Cl2↑ CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl 不变 7.2
CO(NH2)2+H2O B 2Cl--2e-═Cl2↑ CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl 不变 7.2
【解析】
(1)CO2和NH3合成CO(NH2)2,根据元素守恒可知,同时还有H2O生成,配平书写方程式;
(1)CO2和NH3合成CO(NH2)2,根据元素守恒可知,同时还有H2O生成,化学方程式为:2NH3+CO2==CO(NH2)2+H2O,故答案为: 2NH3+CO2==CO(NH2)2+H2O,
①由图可知,左室电极产物为CO2和N2,发生氧化反应,故A为电源的正极,右室电解产物H2,发生还原反应,故B为电源的负极,故答案为:B;
②由图可知,阳极室首先是氯离子放电生成氯气,氯气再氧化尿素生成氮气、二氧化碳,同时会生成HCl,阳极室中发生的反应依次为:2Cl--2e-═Cl2↑ ,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl
故答案为:2Cl--2e-═Cl2↑ ,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl ;
③根据上述反应式可以看出在阴、阳极上产生的OH、H+的数目相等,阳极室中反应产生的H+通过质子交换膜进入阴极室与OH恰好反应生成水,所以阴极室中电解前后溶液的pH不变;
电解收集到的13.44L气体,反应可知生成0.12molN2所消耗的CO(NH2)2的物质的量也为0.12mol,其质量为:m[CO(NH2)2]=0.12mol×60gmol1=7.2g,
故答案为:不变;7.2.

 53天天练系列答案
53天天练系列答案【题目】一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)。
PCl3(g)+Cl2(g)。
编号 | 温度 /℃ | 起始物质 的量/mol | 平衡物质 的量/mol | 达到平衡 所需时间/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t |
Ⅱ | 320 | 0.80 | t1 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t2 |
下列说法正确的是
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C.反应到达平衡时,容器Ⅰ中的平均速率为v(PCl5)=![]() mol·L-1·s-1
mol·L-1·s-1
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行