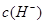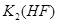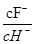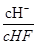题目内容
在蒸馏水中按物质的量之比为1∶1∶1∶2加入AgNO3,Ba(NO3)2,Na2SO4,NaCl,使之完全溶解,以铂电极电解该混合物至溶质完全反应,则所得氧化产物与还原产物的质量比为( )
| A.35.5∶108 | B.71∶2 | C.108∶35.5 | D.71∶109 |
B
【错解分析】四种物质按一定物质的量之比混合、溶解,用惰性电极进行电解。由于①只是片面考虑溶液中阳离子放电顺序是:银离子、氢离子……等;阴离子放电顺序是:氯离子、氢氧根离子……等。②对题目要求溶质完全反应认可有分歧,因此产生以下两种结论。当电路中转移了1mol电子,银离子完全反应,还原产物为1mol银,氧化产物为1mol氯原子(未电解完),氧化产物与还原产物的质量比为35.5∶108(选项A)。当电路中转移了2mol电子,氯离子完全反应,氧化产物为2mol氯原子,还原产物为1mol银和1mol氢原子(水提供),氧化产物与还原产物的质量比为71∶109(选项D)
【正解】反应,生成难溶的氯化银、硫酸钡和硝酸钠。电解质溶液转化为按物质的量之比为3∶1的NaNO3,NaCl,电解时只有氯离子和氢离子参加电极反应,氧化产物与还原产物的质量比为71∶2。

练习册系列答案
相关题目
 溶液加水不断稀释,下列各量始终保持增大的是( )
溶液加水不断稀释,下列各量始终保持增大的是( )