题目内容
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:MnO4-→Mn2+ H2O2→H2O HNO2→NO IO3-→I2如果用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
| A、MnO4- | B、H2O2 | C、HNO2 | D、IO3- |
分析:根据氧化还原反应中得失电子守恒的思想可知,在四个反应中氧化剂不一样,而还原剂均为碘化钾中的碘离子,如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的也就是比较每1mol氧化剂得电子的多少,谁得电子多谁氧化的KI多,生成的I2就多.
解答:解:由氧化还原反应中得失电子守恒,1mol氧化剂得电子越多,生成的I2就多;
1molMnO4-→Mn2+得5mole-,1molH2O2→2H2O得2mole-,1molHNO2→NO得1mole-,1molIO3-→
I2得5mole-,并且还原产物是碘单质,
所以IO3-→I2中1mol氧化剂得电子最多且生成的I2最多,
故选D.
1molMnO4-→Mn2+得5mole-,1molH2O2→2H2O得2mole-,1molHNO2→NO得1mole-,1molIO3-→
| 1 |
| 2 |
所以IO3-→I2中1mol氧化剂得电子最多且生成的I2最多,
故选D.
点评:本题考查了氧化还原反应中电子守恒规律,注意把握元素化合价的变化,本题关键是IO3-由于也被还原为I2,为本题的易错点.同时要求学生具有分析和解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
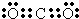
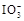 。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食醋;⑥白酒;⑦食糖。你认为进行上述实验时必须使用的物质是 (填序号)。
。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食醋;⑥白酒;⑦食糖。你认为进行上述实验时必须使用的物质是 (填序号)。