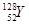题目内容
下列各组微粒中,互为同位素的是( )A.
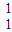 H2和
H2和 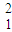 H2
H2B.
 Cl和
Cl和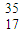 Cl
ClC.O3 和 O2
D.
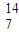 N 和
N 和 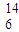 C
C
【答案】分析:质子数相同中子数不同的原子互称同位素.互为同位素原子具有以下特征:质子数相同、化学性质相同、在周期表中的位置相同;中子数不同、质量数不同、物理性质不同;研究对象为原子.
解答:解:A.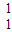 H2和
H2和  H2都是由氢元素组成的,不同氢气分子,结构相同,为同一物质,故A错误;
H2都是由氢元素组成的,不同氢气分子,结构相同,为同一物质,故A错误;
B.1737Cl和 Cl质子数相同为17,中子数不同分别为20、18,是氯元素不同核素,互为同位素,故B正确;
Cl质子数相同为17,中子数不同分别为20、18,是氯元素不同核素,互为同位素,故B正确;
C.O2与O3都是由氧元素形成的结构不同的单质,互为同素异形体,故C错误;
D. N和
N和 C质子数不同,属于不同元素的原子,故D错误.
C质子数不同,属于不同元素的原子,故D错误.
故选B.
点评:本题以同位素为载体,考查化学“五同”比较,难度不大,注意把握概念的理解, H2和
H2和 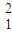 H2是不同分子,但结构相同,为同一物质.
H2是不同分子,但结构相同,为同一物质.
解答:解:A.
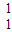 H2和
H2和  H2都是由氢元素组成的,不同氢气分子,结构相同,为同一物质,故A错误;
H2都是由氢元素组成的,不同氢气分子,结构相同,为同一物质,故A错误; B.1737Cl和
 Cl质子数相同为17,中子数不同分别为20、18,是氯元素不同核素,互为同位素,故B正确;
Cl质子数相同为17,中子数不同分别为20、18,是氯元素不同核素,互为同位素,故B正确;C.O2与O3都是由氧元素形成的结构不同的单质,互为同素异形体,故C错误;
D.
 N和
N和 C质子数不同,属于不同元素的原子,故D错误.
C质子数不同,属于不同元素的原子,故D错误.故选B.
点评:本题以同位素为载体,考查化学“五同”比较,难度不大,注意把握概念的理解,
 H2和
H2和 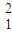 H2是不同分子,但结构相同,为同一物质.
H2是不同分子,但结构相同,为同一物质. 
练习册系列答案
相关题目
 和
和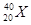 C.D2O和H2O
D.
C.D2O和H2O
D.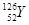 和
和