题目内容
(1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
(2)另一化学探究小组根据SO2中S元素的化合价,预测并通过实验探究验证了SO2的其它性质.探究过程中选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、酸性KMnO4溶液,品红溶液等.探究过程实验装置图如下.请你回答有关问题
①请你完成下面表格
②B中反应的离子方程式为______.
③D中的现象为______.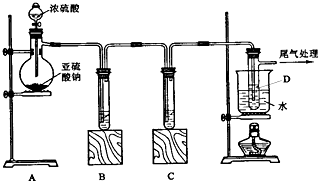
| 物质 | 类别 | 化学性 质预测 |
实验验证(仪器:试管、胶头滴管) | ||
| 实验操作 | 现象 | 实质(离子方程式表示) | |||
| SO2 | 酸性氧化物 | 可以和水反应 | 将盛满二氧化硫气体的试管倒立在水中,并测定试管中溶液的pH | SO2+H2O=H2SO3 | |
| 与碱反应 | 出现白色沉淀 | ||||
①请你完成下面表格
| 装置 | 药品 | 作用 |
| B | 酸性KMnO4溶液 | 验证SO2的还原性 |
| C | ||
| D |
③D中的现象为______.

(1)二氧化硫和水反应生成亚硫酸,导致试管内气体的压强变小,大气压不变,所以试管中水面上升;亚硫酸是酸,所以其水溶液的PH小于7;二氧化硫和澄清的石灰水反应生成不溶于水的亚硫酸钙,离子方程式为SO2+Ca2++2OH-=CaSO3↓+H2O.
故答案为:试管中水面上升,测溶液pH<7(或试管中充满水,溶液呈酸性);
将SO2气体通入澄清石灰水中;SO2+Ca2++2OH-=CaSO3↓+H2O.
(2)①二氧化硫中硫元素的化合价是+4价,属于中间价态,预测其既有氧化性又有还原性.
高锰酸钾有强氧化性,如果二氧化硫能使高锰酸钾褪色,验证二氧化硫有还原性;
硫化钠有还原性,如果二氧化硫和硫化钠反应,验证二氧化硫有氧化性;
如果二氧化硫能使品红溶液褪色,加热又恢复原色,验证SO2使品红褪色的可逆性.
故答案为:
②二氧化硫有还原性,高锰酸钾有氧化性,二氧化硫和高锰酸钾能发生氧化还原反应,
离子方程式为5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+.
故答案为:5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+.
③二氧化硫和有色物质反应生成无色物质,加热后又恢复原色,所以看到的现象是通入SO2气体品红溶液褪色,加热烧杯又溶液又恢复红色.
故答案为:通入SO2气体品红溶液褪色,加热烧杯又溶液又恢复红色.
故答案为:试管中水面上升,测溶液pH<7(或试管中充满水,溶液呈酸性);
将SO2气体通入澄清石灰水中;SO2+Ca2++2OH-=CaSO3↓+H2O.
(2)①二氧化硫中硫元素的化合价是+4价,属于中间价态,预测其既有氧化性又有还原性.
高锰酸钾有强氧化性,如果二氧化硫能使高锰酸钾褪色,验证二氧化硫有还原性;
硫化钠有还原性,如果二氧化硫和硫化钠反应,验证二氧化硫有氧化性;
如果二氧化硫能使品红溶液褪色,加热又恢复原色,验证SO2使品红褪色的可逆性.
故答案为:
| 装置 | 药品 | 探究目的 |
| C | Na2S溶液 | 验证SO2的氧化性 |
| D | 品红溶液 | 验证SO2使品红褪色的可逆性 |
离子方程式为5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+.
故答案为:5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+.
③二氧化硫和有色物质反应生成无色物质,加热后又恢复原色,所以看到的现象是通入SO2气体品红溶液褪色,加热烧杯又溶液又恢复红色.
故答案为:通入SO2气体品红溶液褪色,加热烧杯又溶液又恢复红色.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
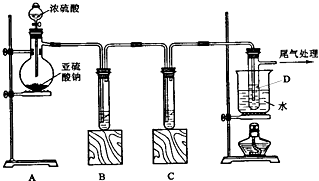 (1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
(1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
| 物质 | 类别 | 化学性 质预测 | 实验验证(仪器:试管、胶头滴管) | ||
| 实验操作 | 现象 | 实质(离子方程式表示) | |||
| SO2 | 酸性氧化物 | 可以和水反应 | 将盛满二氧化硫气体的试管倒立在水中,并测定试管中溶液的pH | SO2+H2O=H2SO3 | |
| 与碱反应 | 出现白色沉淀 | ||||
①请你完成下面表格
| 装置 | 药品 | 作用 |
| B | 酸性KMnO4溶液 | 验证SO2的还原性 |
| C | ||
| D |
③D中的现象为______.
(1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
(2)另一化学探究小组根据SO2中S元素的化合价,预测并通过实验探究验证了SO2的其它性质.探究过程中选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、酸性KMnO4溶液,品红溶液等.探究过程实验装置图如下.请你回答有关问题
①请你完成下面表格
②B中反应的离子方程式为______.
③D中的现象为______.

| 物质 | 类别 | 化学性 质预测 | 实验验证(仪器:试管、胶头滴管) | ||
| 实验操作 | 现象 | 实质(离子方程式表示) | |||
| SO2 | 酸性氧化物 | 可以和水反应 | 将盛满二氧化硫气体的试管倒立在水中,并测定试管中溶液的pH | SO2+H2O=H2SO3 | |
| 与碱反应 | 出现白色沉淀 | ||||
①请你完成下面表格
| 装置 | 药品 | 作用 |
| B | 酸性KMnO4溶液 | 验证SO2的还原性 |
| C | ||
| D |
③D中的现象为______.

(1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
(2)另一化学探究小组根据SO2中S元素的化合价,预测并通过实验探究验证了SO2的其它性质.探究过程中选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、酸性KMnO4溶液,品红溶液等.探究过程实验装置图如下.请你回答有关问题
①请你完成下面表格
②B中反应的离子方程式为______.
③D中的现象为______.

| 物质 | 类别 | 化学性 质预测 | 实验验证(仪器:试管、胶头滴管) | ||
| 实验操作 | 现象 | 实质(离子方程式表示) | |||
| SO2 | 酸性氧化物 | 可以和水反应 | 将盛满二氧化硫气体的试管倒立在水中,并测定试管中溶液的pH | SO2+H2O=H2SO3 | |
| 与碱反应 | 出现白色沉淀 | ||||
①请你完成下面表格
| 装置 | 药品 | 作用 |
| B | 酸性KMnO4溶液 | 验证SO2的还原性 |
| C | ||
| D |
③D中的现象为______.

 (1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
(1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告