题目内容
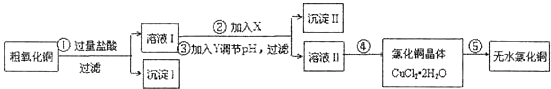
某化学小组拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下图所示:

(1)步骤①中氧化铜与盐酸反应的离子方程式是______________________________。
(2)步骤①、③的过滤操作中,除用到铁架台(带铁圈)外,还需要使用的玻璃仪器是__________。
(3)已知:
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe | 1.9 | 3.2 |
Fe | 7.0 | 9.0 |
Cu | 4.7 | 6.7 |
提供的试剂:a. NaOH b. H | ||
参照表中给出的数据和试剂,请回答:
步骤②的目的是_______________________,反应的离子方程式是_________________。
步骤③中调节溶液pH的范围是__________,试剂Y是__________(填字母)。
(4)在步骤④中所进行的一系列操作是______________________________。
(5)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl![]() ·2H
·2H![]() O,其作用是____________________________________。
O,其作用是____________________________________。
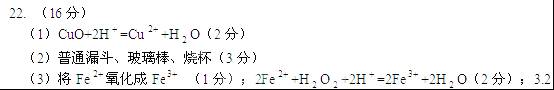
≤pH<4.7(2分);d(1分)
(4)蒸发浓缩,冷却结晶,过滤,洗涤(3分)
(5)干燥的HCl气流既可抑制Cu![]() 的水解,还能带走CuCl
的水解,还能带走CuCl![]() ·2H
·2H![]() O受热产生的水汽(2分)
O受热产生的水汽(2分)


表1 物质沉淀时的pH
物 质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
完全沉淀的pH | 3.7 | 9.6 | 6.4 |
表2 备选试剂
序 号 | A | B | C | D | E |
化学式 | NaOH | CuO | H2O2 | 稀HNO3 | KMnO4 |
回答下列问题:
(1)X_________;Y_________。(填写备选试剂中的序号)
(2)沉淀(Ⅱ)的化学式_____,证明步骤③中沉淀是否完全的操作方法是____________。
(3)第⑤步骤操作中,所需装置如图所示:

按气流从左至右的方向,各装置接口的连接顺序为_________。
D装置的作用是______________________;理由______________________。
某化学小组拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下图所示: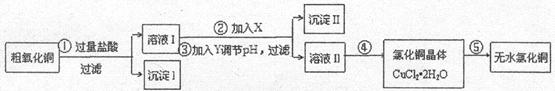
(1)步骤①中氧化铜与盐酸反应的离子方程式是______________________________。
(2)步骤①、③的过滤操作中,除用到铁架台(带铁圈)外,还需要使用的玻璃仪器是__________。
(3)已知:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
Fe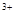 | 1.9 | 3.2 |
Fe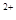 | 7.0 | 9.0 |
Cu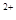 | 4.7 | 6.7 |
提供的试剂:a. NaOH b. H O O c. Na c. Na CO CO d. CuO d. CuO | ||
步骤②的目的是_______________________,反应的离子方程式是_________________。
步骤③中调节溶液pH的范围是__________,试剂Y是__________(填字母)。
(4)在步骤④中所进行的一系列操作是______________________________。
(5)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl
 ·2H
·2H O,其作用是____________________________________。
O,其作用是____________________________________。