题目内容
【题目】除去燃煤烟气中的有毒气体,一直是重要的科研课题。某科研小组设计如下装 置模拟工业脱硫脱氮,探究SO2和NO同时氧化的吸收效果。模拟烟气由N2 (90.02%)、SO2(4.99%)、NO(4.99%)混合而成,各气体的流量分别由流量计控制,调节三路气体相应的流量比例,充分混合后进入A。已知:FeSO4+NO![]() [Fe(NO)]SO4(棕色)
[Fe(NO)]SO4(棕色)
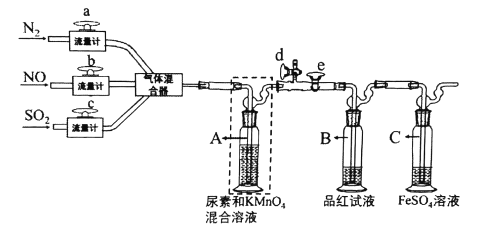
(l)仪器A的名称是____,该装置出气管口有两个玻璃球泡,其作用是____。
(2)反应前装置中需要先通入一段时间N2,目的是____,其操作方法是____。
(3)实验中A瓶出现黑色沉淀,写出 A瓶中脱硫反应的离子方程式____。继续实验,现B瓶溶液颜色不变、C瓶溶液出现棕色,这些现象说明____。
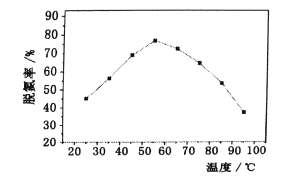
(4)关闭活塞e,打开活塞d,在其出气管口,用NO检测仪研究A在不同温度时的脱氮率,实验结果如下图所示,分析图中信息,得出的结论是____。在55℃之前,脱氮率随温度升高而变化的原因可能是____。
【答案】洗气瓶 消除气泡 排除装置内的空气 关闭d,打开e、a 2H2O+3SO2+2MnO4-=3SO42-+2MnO2↓+4H+或者2CO(NH2)2+4H2O+3SO2+2MnO4-=3SO42-+2MnO2↓+4NH4++2CO2↑ SO2完全吸收,NO不完全吸收 在55℃之前,脱氮率随温度升高而升高,在55℃之后,脱氮率随温度升高而降低。(或者:随温度升高,脱氮率先升高后降低) 温度升高,化学反应速率加快
【解析】
本题以工业脱硫脱氮为载体,考查仪器名称与作用、实验操作与目的等相关知识,从数据、图形和实验现象中提取信息进行实验分析与解释的能力。本题情境来源于真实的工业生产,难度适中
(1)洗气瓶是一种用液体吸收剂通过鼓泡的方式吸收气体中的杂质,达到净化气体作用的一种常用玻璃仪器,实验室可用广口瓶(或锥形瓶、大试管)与长短玻璃管制成简易的洗气装置。鼓泡吸收时,可能有未破裂的气泡进入出气管口堵塞气路,此洗气瓶出气管口有两个玻璃球泡,有消除气泡作用。故答案为:洗气瓶;消除气泡。
(2)O2与NO常温下即可发生反应,SO2在溶液中也可以与O2发生反应,为了避免空气中O2对NO、SO2的吸收或检验产生干扰,实验中需要先关闭d、打开e,形成气体通路,再打开a通入氮气,将整个装置内的空气排走。故答案为:排除装置内的空气;关闭d,打开e、a。答案:排除装置内的空气;关闭d,打开e、a。
(3)高锰酸钾溶液会将NO、SO2氧化成HNO3和H2SO4,高锰酸钾的还原产物为黑色沉淀MnO2,利用尿素水解的氨来中和溶液中生成的酸,避免对实验造成干扰。故方程式为2H2O+3SO2+2MnO4-=3SO42-+2MnO2↓+4H+;或者2CO(NH2)2+4H2O+3SO2+2MnO4-=3SO42-+2MnO2↓+4NH4++2CO2↑。继续实验时,发现B瓶品红溶液颜色不变,说明气体中SO2几乎除净;C瓶溶液硫酸亚铁溶液出现棕色,由题目中的信息可知,NO不完全吸收。故答案为2H2O+3SO2+2MnO4-=3SO42-+2MnO2↓+4H+或者2CO(NH2)2+4H2O+3SO2+2MnO4-=3SO42-+2MnO2↓+4NH4++2CO2↑;SO2完全吸收,NO不完全吸收。
(4)前半段曲线上升,是因为温度促使反应速率加快,也可能是反应中生成的Mn2+自催化作用变强所致;后半段曲线下降,可能温度过高,气体的溶解度降低,影响了气体的溶解吸收,也可能是Mn2+的催化作用变弱所致。故答案为:在55℃之前,脱氮率随温度升高而升高。在55℃之后,脱氮率随温度升高而降低。(或者:随温度升高,脱氮率先升高后降低);在55℃之前,脱氮率随温度升高而变化的原因可能是温度升高,化学反应速率加快。

【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)①④⑥三种元素构成的化合物的电子式:__;⑨的最高价氧化物对应水化物的化学式:__。
(2)⑤、⑦、⑧的简单离子半径由大到小的顺序:__(用离子符号填写)。
(3)用一个化学方程式表示④、⑤二种元素非金属性的强弱__。
(4)⑦的单质与⑥的最高价氧化物对应水化物的水溶液反应的离子方程式为__。
(5)元素①、元素④以原子个数比为1∶1形成化合物Q,元素①、元素③形成化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终产物对空气没有污染,写出该反应的化学方程式:__。