题目内容
(16分)硅单质及其化合物应用范围很广。请回答下列问题:
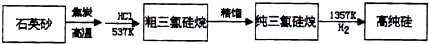
制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
(1)在制粗硅的反应中,焦炭的作用是 。
(2)整个制备过程必须严格控制无水、无氧。
①SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式 ;②H2还原SiHCl3过程中若混O2,可能引起的后果是 。
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡。写出实验现象并给予解释 。
(16分)
(1)作还原剂,与石英砂中的SiO2反应,生成单质Si。(2分)
(2)①SiHCl3+3H2O===H2SiO3+3HCl +H2↑(4分)
②反应体系中有大量H2,高温下,H2遇O2易发生爆炸;氧气可能会氧化SiHCl3。(4分)
(3)试管中有白色胶状沉淀生成,同时有刺激性气味气体生成;Na2SiO3和NH4Cl均能够水解,二者互相促进,Na2SiO3水解生成H2SiO3,NH4Cl水解产生NH3。(6分)
解析:

练习册系列答案
相关题目


 iCl4液体经精馏提纯后与过量H2在1100 ℃~1200 ℃ 反应制得纯硅
iCl4液体经精馏提纯后与过量H2在1100 ℃~1200 ℃ 反应制得纯硅
 。
。