题目内容
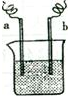 (2009?南平二模)图中,两电极上发生的电极反应为:a极:Cu2++2e-=Cu b极:Fe-2e-=Fe2+,下列说法中不正确的是( )
(2009?南平二模)图中,两电极上发生的电极反应为:a极:Cu2++2e-=Cu b极:Fe-2e-=Fe2+,下列说法中不正确的是( )分析:由a极:Cu2++2e-=Cu,b极:Fe-2e-=Fe2+,b极发生氧化反应,a极发生还原反应,则该装置可能为原电池或电解池,利用化合价的变化来分析电极反应,以此来解答.
解答:解:A.由图可知,该装置可能有外加电源,则可能为电解池,故A正确;
B.a极上Cu元素的化合价降低,则发生还原反应,故B正确;
C.该装置为电解池时,a、b可以为同种电极材料,故C正确;
D.在原电池中,b为负极,在电解池中b为阳极,则该装置在工作时,溶液中的阳离子可能向a极移动,故D错误;
故选D.
B.a极上Cu元素的化合价降低,则发生还原反应,故B正确;
C.该装置为电解池时,a、b可以为同种电极材料,故C正确;
D.在原电池中,b为负极,在电解池中b为阳极,则该装置在工作时,溶液中的阳离子可能向a极移动,故D错误;
故选D.
点评:本题考查原电池和电解池,利用氧化还原反应来分析电极反应是解答本题的关键,并熟悉工作原理来解答,难度不大.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目