题目内容
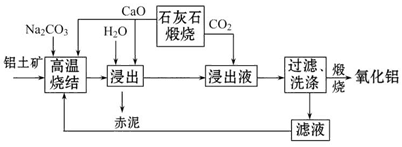
烧结法制氧化铝生产过程如下:
已知:
①铝土矿主要成分为:Al2O3、SiO2、Fe2O3和TiO2。
②高温烧结时,Al2O3、Fe2O3、TiO2都能发生反应分别生成NaAlO2、Na2Fe2O4和难溶于水的CaTiO3。
请回答下列问题:
(1)Na2Fe2O4遇水便发生水解反应生成Fe(OH)3,写出Na2Fe2O4水解的化学方程式____________。
(2)浸出时再加入CaO的目的是______________________________________。
(3)浸出液中发生的生成Al(OH)3的离子方程式为____________________________________。
(4)滤液的主要成分是_________(写化学式);滤液循环使用的优点有________ (任答一点)。

已知:
①铝土矿主要成分为:Al2O3、SiO2、Fe2O3和TiO2。
②高温烧结时,Al2O3、Fe2O3、TiO2都能发生反应分别生成NaAlO2、Na2Fe2O4和难溶于水的CaTiO3。
请回答下列问题:
(1)Na2Fe2O4遇水便发生水解反应生成Fe(OH)3,写出Na2Fe2O4水解的化学方程式____________。
(2)浸出时再加入CaO的目的是______________________________________。
(3)浸出液中发生的生成Al(OH)3的离子方程式为____________________________________。
(4)滤液的主要成分是_________(写化学式);滤液循环使用的优点有________ (任答一点)。
(1)Na2Fe2O4+4H2O=2NaOH+2Fe(OH)3↓
(2)除去可能溶于水的硅酸盐,提高氧化铝纯度
(3)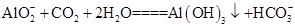
(4)NaHCO3、Ca(HCO3)2 减少工业废水排放或节约原料,降低成本(其他合理答案也可)
(2)除去可能溶于水的硅酸盐,提高氧化铝纯度
(3)
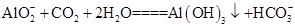
(4)NaHCO3、Ca(HCO3)2 减少工业废水排放或节约原料,降低成本(其他合理答案也可)
(1)由题设知,Na2Fe2O4和水是反应物,Fe(OH)3是生成物,则Na2Fe2O4水解反应的化学方程式为:Na2Fe2O4+4H2O=2NaOH+2Fe(OH)3↓。
(2)由于浸出液中可能还含有可溶性硅酸盐,再加入CaO的目的是:除去可能溶于水的硅酸盐,提高氧化铝纯度。
(3)由于浸出液的主要成分是NaAlO2,通入过量CO2气体发生反应的离子方程式为: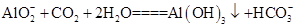 。
。
(4)滤液的主要成分为:NaHCO3和Ca(HCO3)2,滤液循环使用的优点有:①减少工业废水排放;②节约原料,降低成本等。
(2)由于浸出液中可能还含有可溶性硅酸盐,再加入CaO的目的是:除去可能溶于水的硅酸盐,提高氧化铝纯度。
(3)由于浸出液的主要成分是NaAlO2,通入过量CO2气体发生反应的离子方程式为:
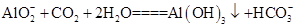 。
。(4)滤液的主要成分为:NaHCO3和Ca(HCO3)2,滤液循环使用的优点有:①减少工业废水排放;②节约原料,降低成本等。

练习册系列答案
相关题目
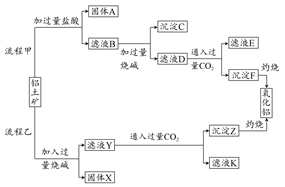
 4AlCl3(g)+3O2(g) ΔH>0 。下列分析错误的是( )
4AlCl3(g)+3O2(g) ΔH>0 。下列分析错误的是( ) xFe2O3的铝灰制备Al2(S04)3
xFe2O3的铝灰制备Al2(S04)3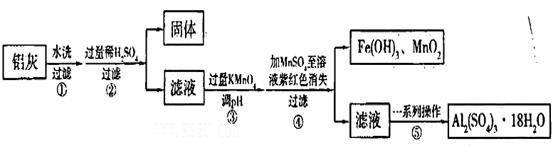
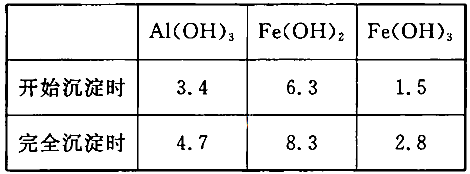
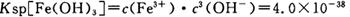 当pH=2时,Fe3+开始沉淀的浓度为_______________。
当pH=2时,Fe3+开始沉淀的浓度为_______________。