题目内容
下列实验现象与结论相符合的是
- A.在溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则溶液中一定存在SO42-
- B.在铝热剂加入少量稀盐酸,再迅速滴加KSCN溶液,未出现血红色;无法判断铝热剂中是否含有Fe2O3
- C.某盐焰色反应火焰为黄色,则该盐金属元素一定只有钠元素
- D.如图所示,放置一段时间后,饱和CuSO4溶液中出现蓝色晶体,说明CaO有一定的脱水性
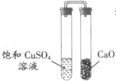
B
分析:A、与BaCl2溶液反应出现的白色沉淀,可以是硫酸钡也可以是氯化银;
B、亚铁离子,遇到KSCN溶液不会出现血红色,铝和三价铁能反应生成亚铁离子;
C、钠元素的焰色反应为黄色;
D、CaO有一定的吸水性,浓硫酸有脱水性.
解答:A、在溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则溶液中SO42-,可能存在Ag+,可能二者均存在,故A错误;
B、铝热剂是把铝粉和三氧化二铁粉末按一定比例配成的呈粉红色的混合物,向其中加入少量稀盐酸,氧化铁生成三价铁离子,由于盐酸不足,反应完后铝有剩余,就能将三价铁还原为二价铁,如果此时铝还有过量,则二价铁被进一步还原成铁单质,这些都不会与KSCN发生络合反应而出现血红色,而过量的氧化铁固体也是不会与KSCN反应的,只有离子态的三价铁才能与它反应,故B正确;
C、钠元素的焰色反应为黄色,无法排除钾离子是否存在,因为钾离子的焰色为紫色,如果没有透过蓝色钴玻璃观察,钠离子产生的黄色会使紫色难以观察,故C错误;
D、CaO有一定的吸水性,不是脱水性,故D错误.
故选B.
点评:本题主要考查了学生有关物质的鉴别知识,可以根据所学内容来分析.
分析:A、与BaCl2溶液反应出现的白色沉淀,可以是硫酸钡也可以是氯化银;
B、亚铁离子,遇到KSCN溶液不会出现血红色,铝和三价铁能反应生成亚铁离子;
C、钠元素的焰色反应为黄色;
D、CaO有一定的吸水性,浓硫酸有脱水性.
解答:A、在溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则溶液中SO42-,可能存在Ag+,可能二者均存在,故A错误;
B、铝热剂是把铝粉和三氧化二铁粉末按一定比例配成的呈粉红色的混合物,向其中加入少量稀盐酸,氧化铁生成三价铁离子,由于盐酸不足,反应完后铝有剩余,就能将三价铁还原为二价铁,如果此时铝还有过量,则二价铁被进一步还原成铁单质,这些都不会与KSCN发生络合反应而出现血红色,而过量的氧化铁固体也是不会与KSCN反应的,只有离子态的三价铁才能与它反应,故B正确;
C、钠元素的焰色反应为黄色,无法排除钾离子是否存在,因为钾离子的焰色为紫色,如果没有透过蓝色钴玻璃观察,钠离子产生的黄色会使紫色难以观察,故C错误;
D、CaO有一定的吸水性,不是脱水性,故D错误.
故选B.
点评:本题主要考查了学生有关物质的鉴别知识,可以根据所学内容来分析.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
下列实验现象与结论相符合的是( )
| A、在溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则溶液中一定存在SO42- | B、在铝热剂加入少量稀盐酸,再迅速滴加KSCN溶液,未出现血红色;无法判断铝热剂中是否含有Fe2O3 | C、某盐焰色反应火焰为黄色,则该盐金属元素一定只有钠元素 | D、如图所示,放置一段时间后,饱和CuSO4溶液中出现蓝色晶体,说明CaO有一定的脱水性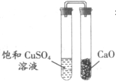 |