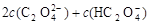题目内容
草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol/L NaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH)="=" 0时,c(H+,W)="=" 1 × 10-2 mol/L |
B.V(NaOH)< 10 mL时,不可能存在c(Na+)="=" 2 c(C2O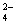 )+ c(HC2O )+ c(HC2O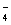 ) ) |
| C.V(NaOH)="=" 10 mL时,c(H+,W)="=" 1 × 10-7mol/L |
D.V(NaOH)> 10 mL时,c(Na+)> c(C2O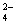 )>c(HC2O )>c(HC2O ) ) |
D
解析试题分析:草酸是二元中强酸,草酸氢钠溶液显酸性,这说明HC2O4-的水解程度小于HC2O4-的电离程度,但电离是不彻底的,所以溶液中氢离子的浓度小于0.01mol/L,A不正确;当V(NaOH)="=" 10 mL时,二者恰好反应时生成草酸钠,水解溶液显碱性。根据电荷守恒可知c(H+)+c(Na+)=" 2" c(C2O )+ c(HC2O
)+ c(HC2O )+c(OH-),如果V(NaOH)< 10 mL,则溶液就可能显中性,则c(H+)=c(OH-),所以c(Na+)="=" 2 c(C2O
)+c(OH-),如果V(NaOH)< 10 mL,则溶液就可能显中性,则c(H+)=c(OH-),所以c(Na+)="=" 2 c(C2O )+ c(HC2O
)+ c(HC2O ),即B、C都不正确,选项D正确,答案选D。
),即B、C都不正确,选项D正确,答案选D。
考点:考查溶液中离子浓度大小比较以及溶液酸碱性的判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识的巩固和训练的同时,侧重对学生基础知识的巩固和训练,有利于调动学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是利用好几种守恒关系即电荷守恒、物料守恒和质子守恒,然后结合题意灵活运用即可。

练习册系列答案
相关题目