题目内容
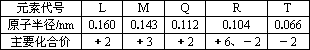
根据部分短周期元素的原子半径及主要化合价信息,判断以下叙述正确的是( )
|
分析:L和Q的化合价都为+2价,应为周期表第ⅡA族,根据半径关系可知Q为Be,L为Mg;R和T的化合价都有-2价,应为周期表第ⅥA族元素,R的最高价为+6价,应为S元素,T无正价,应为O元素;M的化合价为+3价,应为周期表第ⅢA族元素,根据M原子半径大于R小于L可知应和L同周期,为Al元素,结合元素周期律知识解答该题.
解答:解:L和Q的化合价都为+2价,应为周期表第ⅡA族,根据半径关系可知Q为Be,L为Mg;R和T的化合价都有-2价,应为周期表第ⅥA族元素,R的最高价为+6价,应为S元素,T无正价,应为O元素;M的化合价为+3价,应为周期表第ⅢA族元素,根据M原子半径大于R小于L可知应和L同周期,为Al元素.
A.水分子之间存在氢键,常温下水为液体,硫化氢为气体,故水的沸点更高,故A错误;
B.同主族自上而下金属性增强,故金属性为Be<Mg,故B错误;
C.M与T形成的化合物是氧化铝,其化学式是Al2O3,故C正确;
D.Mg2+核外有10个电子,S2-核外有18个电子,二者核外电子数不同,故D错误,
故选C.
A.水分子之间存在氢键,常温下水为液体,硫化氢为气体,故水的沸点更高,故A错误;
B.同主族自上而下金属性增强,故金属性为Be<Mg,故B错误;
C.M与T形成的化合物是氧化铝,其化学式是Al2O3,故C正确;
D.Mg2+核外有10个电子,S2-核外有18个电子,二者核外电子数不同,故D错误,
故选C.
点评:本题考查元素位置结构和性质的关系及应用,题目难度中等,正确把握元素化合价、原子半径与元素性质的关系是解答该题的关键,注意元素周期律的递变规律的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
|
根据部分短周期元素的原子半径及主要化合价信息,判断以下叙述正确的是
| |
| [ ] | |
A. |
氢化物的沸点为H2T<H2R |
B. |
金属性强弱:L<Q |
C. |
M与T形成的化合物的化学式是Al2O3 |
D. |
L2+与R2-的核外电子数相等 |
根据部分短周期元素的原子半径及主要化合价信息,判断以下叙述正确的是
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
|
主要化合价 |
+2 |
+3 |
+2 |
+6、—2 |
—2 |
A.氢化物的沸点为H2T<H2R B.金属性强弱:L<Q
C.M与T形成的化合物的化学式是Al2O3 D.L2+与R2-的核外电子数相等
根据部分短周期元素的原子半径及主要化合价信息,判断以下叙述正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、—2 | —2 |
A.氢化物的沸点为H2T<H2R B.金属性强弱:L<Q
C.M与T形成的化合物的化学式是Al2O3 D.L2+与R2-的核外电子数相等