题目内容
下列反应离子方程式正确的是 ( )
A.将少量二氧化硫气体通入次氯酸钠溶液中 : SO2+2ClO-+H2O=SO32-+2HClO
B.向苯酚钠溶液中通入二氧化碳:CO2+H2O+2C6H5O-→2C6H5OH+CO32-
C.向明矾溶液中滴加Ba(OH)2,恰好使SO42-沉淀完全:2A13++3SO42-+ 3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
D.向氯化铝溶液中投入过量Na:Al3++4Na+2H2O=AlO-2+4Na++2H2↑
D
【解析】略

(10分)X、Y、Z三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42—、OH- |
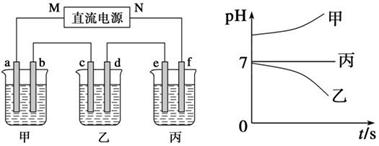
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放250 mL足量的X溶液、足量的Y溶液、足量的Z溶液,电极均为石墨电极。
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的________极(填写“正”或“负”)。
(2)甲烧杯中电极b上发生的电极反应为 。
(3)乙烧杯电解的总反应离子方程式为_________________________________,电解一段时间后停止电解(此时溶液中还有原溶质),若要将乙烧杯中的溶液恢复到原状态,则需要加入 (填化学式)。
(4)若经过一段时间后,丙装置中两极附近均滴酚酞, _______极附近变红,其原因是
。
(10分)X、Y、Z三种强电解质,它们在水中电离出的离子如下表所示:
|
阳离子 |
Na+、K+、Cu2+ |
|
阴离子 |
SO42—、OH- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放250 mL足量的X溶液、足量的Y溶液、足量的Z溶液,电极均为石墨电极。
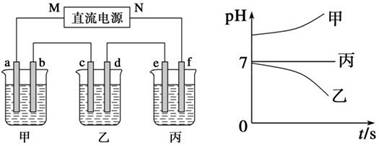
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的________极(填写“正”或“负”)。
(2)甲烧杯中电极b上发生的电极反应为 。
(3)乙烧杯电解的总反应离子方程式为_________________________________,电解一段时间后停止电解(此时溶液中还有原溶质),若要将乙烧杯中的溶液恢复到原状态,则需要加入 (填化学式)。
(4)若经过一段时间后,丙装置中两极附近均滴酚酞, _______极附近变红,其原因是
。[来源:学_科_网]