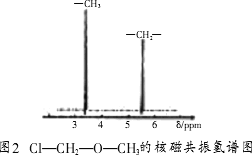
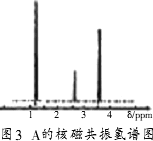
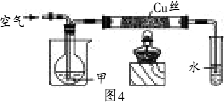
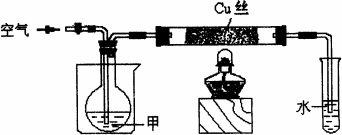
题目内容
图中,甲由C、H、O三种元素组成,元素的质量比为12:3:8,甲的沸点为78.5℃,其蒸气与H2的相对密度是23.将温度控制在400℃以下,按要求完成实验.
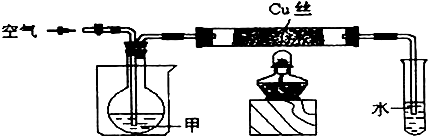
(1)在通入空气的条件下进行实验Ⅰ.
①甲的名称是
a.打开活塞
b.用鼓气气球不断鼓入空气
c.点燃酒精灯给铜丝加热
②实验结束,取试管中的溶液与新制的Cu(OH)2混合,加热至沸腾,实验现象为
(2)在停止通入空气的条件下进行实验Ⅱ.
①关闭活塞,为使甲持续进入反应管中,需要进行的操作是
②甲蒸气进入反应管后,在铜做催化剂有250-350℃条件下发生可逆的化学反应,在试管中收集到了实验Ⅰ相同的产物,并有可燃性气体单质放出.该反应揭示了甲催化氧化的本质.写出实验Ⅱ中反应的化学方程式
(3)甲也是一种良好的有机溶剂.某同学在进行溴乙烷与NaOH的甲溶液的反应中,观察到有气体生成.请设计一种实验方案检验该气体,完成下列表格.

(1)在通入空气的条件下进行实验Ⅰ.
①甲的名称是
乙醇
乙醇
,加入药品后的操作依次是cab或acb
cab或acb
.a.打开活塞
b.用鼓气气球不断鼓入空气
c.点燃酒精灯给铜丝加热
②实验结束,取试管中的溶液与新制的Cu(OH)2混合,加热至沸腾,实验现象为
有砖红色沉淀生成
有砖红色沉淀生成
写出发生反应的化学方程式CH3CHO+2Cu(OH)2
CH3COOH+Cu2O+2H2O
| △ |
CH3CHO+2Cu(OH)2
CH3COOH+Cu2O+2H2O
| △ |
(2)在停止通入空气的条件下进行实验Ⅱ.
①关闭活塞,为使甲持续进入反应管中,需要进行的操作是
向烧杯中加入水,在78.5℃以上温度加热
向烧杯中加入水,在78.5℃以上温度加热
.②甲蒸气进入反应管后,在铜做催化剂有250-350℃条件下发生可逆的化学反应,在试管中收集到了实验Ⅰ相同的产物,并有可燃性气体单质放出.该反应揭示了甲催化氧化的本质.写出实验Ⅱ中反应的化学方程式
CH3CH2OH
CH3CHO+H2
| 250-350℃ |
| Cu |
CH3CH2OH
CH3CHO+H2
,并结合该化学方程式简要说明实验Ⅰ中所通空气的作用| 250-350℃ |
| Cu |
使氢气和氧气结合生成水,使平衡向正反应方向移动
使氢气和氧气结合生成水,使平衡向正反应方向移动
(3)甲也是一种良好的有机溶剂.某同学在进行溴乙烷与NaOH的甲溶液的反应中,观察到有气体生成.请设计一种实验方案检验该气体,完成下列表格.
| 操作方法及所用试剂 | 实验现象 |
洗气、水 洗气、水 |
酸性高锰酸钾溶液褪色 酸性高锰酸钾溶液褪色 |
分析:(1)甲由C、H、O三种元素组成,元素的质量比为12:3:8,则N(C):N(H):N(O)=
:
:
=2:6:1,则最简式为C2H6O,其蒸气与H2的相对密度是23,可知相对分子质量为46,则甲的分子式为C2H6O,可在铜丝作用下与氧气反应,应为乙醇,在铜为催化剂条件下加热,与氧气发生氧化还原反应生成乙醛反应为2CH3CH2OH+O2
2CH3CHO+2H2O,乙醛可与新制氢氧化铜浊液在加热条件下发生氧化还原反应生成乙酸和氧化亚铜,反应的方程式为CH3CHO+2Cu(OH)2
CH3COOH+Cu2O+2H2O,
(2)可用水浴加热的方法使乙醇挥发,提供乙醇气体,由②题意可以乙醇在铜作催化剂作用下生成乙醛和氢气,从平衡移动的角度分析通入空气的作用;
(3)溴乙烷在氢氧化钠的乙醇溶液中发生消去反应生成乙烯,因乙醇易挥发,可将气体通入水中,除去乙醇,然后用酸性高锰酸钾溶液检验.
| 12 |
| 12 |
| 3 |
| 1 |
| 8 |
| 16 |
| 催化剂 |
| △ |
| △ |
(2)可用水浴加热的方法使乙醇挥发,提供乙醇气体,由②题意可以乙醇在铜作催化剂作用下生成乙醛和氢气,从平衡移动的角度分析通入空气的作用;
(3)溴乙烷在氢氧化钠的乙醇溶液中发生消去反应生成乙烯,因乙醇易挥发,可将气体通入水中,除去乙醇,然后用酸性高锰酸钾溶液检验.
解答:解:(1)①甲由C、H、O三种元素组成,元素的质量比为12:3:8,则N(C):N(H):N(O)=
:
:
=2:6:1,则最简式为C2H6O,其蒸气与H2的相对密度是23,可知相对分子质量为46,则甲的分子式为C2H6O,可在铜丝作用下与氧气反应,应为乙醇,加入药品后,可先打开活塞,然后点燃酒精灯给铜丝加热,最后用鼓气气球不断鼓入空气,或先打开活塞,再点燃酒精灯给铜丝加热,最后用鼓气气球不断鼓入空气,
故答案为:乙醇;cab或acb;
②实验结束,取试管中的溶液与新制的Cu(OH)2混合,加热至沸腾,乙醛可与新制氢氧化铜浊液在加热条件下发生氧化还原反应生成乙酸和砖红色的氧化亚铜,反应的方程式为CH3CHO+2Cu(OH)2
CH3COOH+Cu2O+2H2O,
故答案为:有砖红色沉淀生成;CH3CHO+2Cu(OH)2
CH3COOH+Cu2O+2H2O;
(2)①可用水浴加热的方法使乙醇挥发,提供乙醇气体,水浴加热时,温度应在78.5℃以上,以使乙醇挥发,
故答案为:向烧杯中加入水,在78.5℃以上温度加热;
②乙醇在铜作催化剂作用下生成乙醛和氢气,反应的方程式为CH3CH2OH
CH3CHO+H2,因反应为可逆反应,可知实验Ⅰ中所通空气的作用是使氢气和氧气结合生成水,使平衡向正反应方向移动,
故答案为:CH3CH2OH
CH3CHO+H2;使氢气和氧气结合生成水,使平衡向正反应方向移动;
(3)溴乙烷在氢氧化钠的乙醇溶液中发生消去反应生成乙烯,因乙醇易挥发,可将气体通入水中,除去乙醇,然后用酸性高锰酸钾溶液检验,
故答案为:
| 12 |
| 12 |
| 3 |
| 1 |
| 8 |
| 16 |
故答案为:乙醇;cab或acb;
②实验结束,取试管中的溶液与新制的Cu(OH)2混合,加热至沸腾,乙醛可与新制氢氧化铜浊液在加热条件下发生氧化还原反应生成乙酸和砖红色的氧化亚铜,反应的方程式为CH3CHO+2Cu(OH)2
| △ |
故答案为:有砖红色沉淀生成;CH3CHO+2Cu(OH)2
| △ |
(2)①可用水浴加热的方法使乙醇挥发,提供乙醇气体,水浴加热时,温度应在78.5℃以上,以使乙醇挥发,
故答案为:向烧杯中加入水,在78.5℃以上温度加热;
②乙醇在铜作催化剂作用下生成乙醛和氢气,反应的方程式为CH3CH2OH
| 250-350℃ |
| Cu |
故答案为:CH3CH2OH
| 250-350℃ |
| Cu |
(3)溴乙烷在氢氧化钠的乙醇溶液中发生消去反应生成乙烯,因乙醇易挥发,可将气体通入水中,除去乙醇,然后用酸性高锰酸钾溶液检验,
故答案为:
| 操作方法及所用试剂 | 实验现象 |
| 洗气、水 | 酸性高锰酸钾溶液褪色 |
点评:本题综合有机物化学反应原理的探究,侧重于学生的计算能力、分析能力、实验能力和评价能力,为高考常见题型,难度较大,注意把握题给信息,为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
| |||||||||||
 由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中甲、乙、丙是单质,X、Y是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.以下判断错误的是( )
由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中甲、乙、丙是单质,X、Y是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.以下判断错误的是( )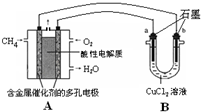 (2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.
(2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.