题目内容
【题目】相对分子质量为M的气态化合物VL(标准状况)溶于mg水中,得到溶液的质量分数为ω%,物质的量浓度cmol/L,密度为ρg/cm3,则下列说法正确的是
A. 相对分子质量M可表示为:![]()
B. 溶液密度ρ可表示为:![]()
C. 溶液的质量分数ω%可表示为:![]()
D. 物质的量浓度C可表示为:![]()
【答案】A
【解析】
A、mg:m(溶质)=(1-ω%):ω%,所以m(溶质)=![]() g,所以
g,所以![]() ×Mg/mol=
×Mg/mol=![]() g,解得M=
g,解得M=![]() ,所以该气体的相对分子质量为
,所以该气体的相对分子质量为![]() ,选项A正确;B、由于c=
,选项A正确;B、由于c=![]() ,所以ρ=
,所以ρ=![]() =
=![]() ,选项B错误; C、溶质的质量为
,选项B错误; C、溶质的质量为![]() ×Mg/mol =
×Mg/mol =![]() g,溶液质量为mg+
g,溶液质量为mg+![]() ×Mg/mol=(m+
×Mg/mol=(m+![]() )g,所以质量分数为
)g,所以质量分数为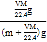 =
=![]() ,选项C错误;D、溶质的物质的量为以
,选项C错误;D、溶质的物质的量为以![]() =
=![]() mol,溶液质量为mg+
mol,溶液质量为mg+![]() ×Mg/mol=(m+
×Mg/mol=(m+![]() )g,所以溶液的体积为
)g,所以溶液的体积为![]() ,所以溶液浓度为
,所以溶液浓度为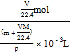 =
=![]() mol/L,选项D错误;答案选A。
mol/L,选项D错误;答案选A。

练习册系列答案
相关题目