题目内容
海洋中资源丰富,以海水为原料可制得一系列产品,如下图所示: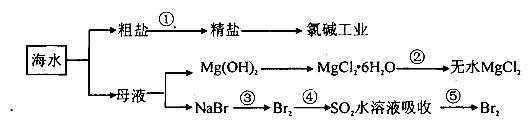
下列有关说法正确的是
| A.第①步除去粗盐SO42-、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
B.将第②步结晶出的MgCl2 6H2O在空气中加热分解制备无水MgCl2 6H2O在空气中加热分解制备无水MgCl2 |
| C.在第③④⑤步中溴元素均被氧化 |
| D.电解饱和食盐水时,在阴极区生成NaOH |
D
解析试题分析:A、Ca2+用碳酸钠除去,Mg2+、Fe3+用氢氧化钠除去,SO42-用氯化钡除去,最后加入盐酸酸化。但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,所以选项A不正确;B、由于镁离子在溶液中存在水解平衡Mg2++H2O Mg(OH)2+2H+,水解吸热,加热促进水解,且生成的氯化氢极易挥发,所以加热氯化镁晶体得到氢氧化镁,因此将第②步结晶出的MgCl2
Mg(OH)2+2H+,水解吸热,加热促进水解,且生成的氯化氢极易挥发,所以加热氯化镁晶体得到氢氧化镁,因此将第②步结晶出的MgCl2 6H2O在氯化氢气流中加热分解制备无水MgCl2,B不正确;C、单质溴与SO2反应的方程式为Br2+SO2+2H2O=H2SO4+2HBr,反应中溴元素化合价从0价降低到-1价,得到电子,被还原,而在反应③⑤中溴元素的化合价均从-1价升高到0价,失去电子,被氧化,C不正确;D、电解池中阳极失去电子,阴极得到电子。所以用惰性电极电解饱和食盐水阴极是氢离子放电放出氢气,同时破坏阴极周围水的电离平衡,所以氢氧化钠在阴极生成,D正确,答案选D。
6H2O在氯化氢气流中加热分解制备无水MgCl2,B不正确;C、单质溴与SO2反应的方程式为Br2+SO2+2H2O=H2SO4+2HBr,反应中溴元素化合价从0价降低到-1价,得到电子,被还原,而在反应③⑤中溴元素的化合价均从-1价升高到0价,失去电子,被氧化,C不正确;D、电解池中阳极失去电子,阴极得到电子。所以用惰性电极电解饱和食盐水阴极是氢离子放电放出氢气,同时破坏阴极周围水的电离平衡,所以氢氧化钠在阴极生成,D正确,答案选D。
考点:考查粗盐提纯、镁离子水解、氧化还原反应以及电解产物的判断

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
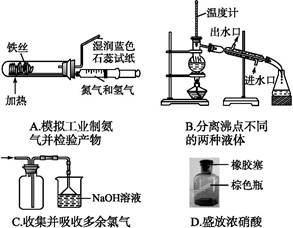
下列实验方法正确的是
| A.配制一定物质的量浓度的溶液时,若加水超过容量瓶的刻度线,用胶头滴管将多余液体吸出即可 |
| B.区别Na2CO3和NaHCO3时,可将它们分别和Ca(OH)2溶液混合,看有无沉淀产生 |
| C.区别FeCl3溶液和Fe(OH)3胶体时,可将它们分别用一束光照射,看有无丁达尔效应出现 |
| D.检验某溶液中是否含有NH4+离子时,可加入适量的氢氧化钠溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体即可 |
实验室保存下列物质的方法中,不正确的是
| A.少量金属钠保存在煤油里 |
| B.烧碱溶液盛装在用玻璃塞塞紧的试剂瓶中 |
| C.FeSO4溶液存放在加有少量铁粉的试剂瓶中 |
| D.氯水应装在棕色瓶中密封避光保存 |
某研究性学习小组讨论甲、乙、丙、丁四种实验装置的有关用法,其中不正确的是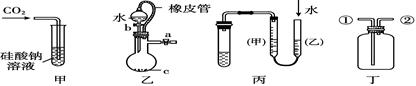
| A.甲装置:可用来证明碳的非金属性比硅强 |
| B.乙装置:橡皮管的作用是使水能顺利流下 |
| C.丙装置:用图示的方法不能检查此装置的气密性 |
| D.丁装置:从①口进气可收集二氧化碳,从②口进气可收集氢气 |
在实验室进行下列实验, 括号内的实验用品都能用到的是( )
| A.硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体) |
| B.蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液) |
| C.钠的焰色反应(铂丝、氯化钠溶液、稀盐酸) |
| D.肥皂的制取(蒸发皿、玻璃棒、甘油) |
下列实验操作中,主要不是从安全因素考虑的是 ( )。
A.用NH4Cl、Ca(OH)2制备NH3时,可用如图所示装置吸收尾气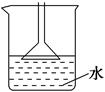 |
| B.制备Fe(OH)2时,吸有NaOH溶液的胶头滴管要插入亚铁盐溶液中再挤出NaOH溶液 |
| C.加热试管中的固体时,试管口应略向下倾斜 |
| D.用氢气还原氧化铜时,先通一会氢气,再加热氧化铜 |
在实验室中进行下列实验探究,其中的实验用品均能用到且正确的是( )。
| 选项 | 实验探究内容 | 实验用品 |
| A | 铜丝在氯气中燃烧 | 坩埚钳、燃烧匙、氯气、铜丝 |
| B | 铝热反应 | 铁架台、大蒸发皿、普通漏斗、铝粉、Fe2O3 |
| C | 实验室制备氨气 | 试管、集气瓶、酒精灯、NH4Cl、Ca(OH)2 |
| D | 用KMnO4晶体配制500 mL 0.1 mol·L-1 KMnO4溶液 | 容量瓶、烧杯、玻璃棒、酸式滴定管、KMnO4 |
对实验Ⅰ~Ⅳ的实验现象预测正确的是( )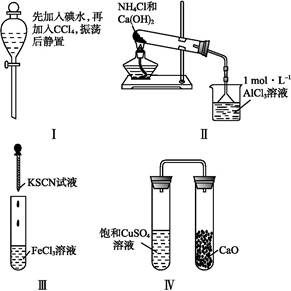
| A.实验Ⅰ:液体分层,下层呈无色 |
| B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C.实验Ⅲ:试管中立刻出现红色沉淀 |
| D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |