题目内容
下列实验操作正确且能达到目的是( )
| A.将AlCl3溶液蒸发结晶提取无水AlCl3 |
| B.在温水瓶中加入Na2CO3溶液泡浸后加入盐酸能除去内壁的CaSO4 |
| C.在淀粉溶液中加入适量稀硫酸微热,再加少量新制Cu(OH)2悬浊液并加热,产生红色沉淀 |
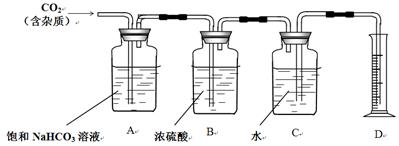
| D.将Cl2、HCl混合气体通过盛有NaHCO3饱和溶液的洗气瓶除去HCl |
B
试题分析:AlCl3 为强酸弱碱盐,蒸发结晶容易大量水解,同时水解产生挥发性的酸HCl,导致蒸发结晶后得不到无水AlCl3 ,A错误;CaSO4 存在溶解平衡,加入饱和Na2CO3 溶液,CO32- 与Ca2+ 结合生成更难溶的CaCO3 沉淀,从而除去了内壁的CaSO4 ,B正确;淀粉在酸性条件下水解后,不能直接加新制Cu(OH)2悬浊液进行检验,应该先加入碱中和水解的酸,所以C错误;除去Cl2 中混有的HCl气体,应该通过饱和的食盐水洗气瓶,D错误;故选B。

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目