题目内容
海洋中含有丰富的资源,是人类的巨大宝库.我国拥有很长的海岸线,东部沿岸海滩平缓,多细沙,日照时间长,不少盐场均集中于此.回答下列问题:
(1)制海盐方法如下:海水涨潮时,将海水引入盐田,等落潮时,再用日晒的方法,待盐田水分蒸发到一定程度时,再撒入食盐颗粒(称为晶种),食盐晶体即从饱和溶液中析出.请说明盐田获得食盐晶体的条件________.
(2)以食盐为主要原料可以制备纯碱.试用化学方程式表示其制备过程:
________.
此法制得的纯碱中常含有少量氯化钠,要测定样品中的纯碱的质量分数,还可采用下图中的装置进行实验:
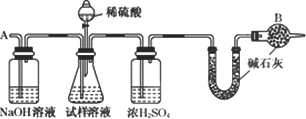
请你用一句话叙述该实验设计的基本原理:________.
(3)氯碱化工厂制得的烧碱中也含有少量氯化钠(假设不含其他杂质),用中和滴定法设计一个实验方案以测定样品中烧碱和氯化钠的质量分数.试剂是0.100 0 mol/L盐酸、酚酞溶液,仪器是50 mL的酸式滴定管、锥形瓶.其实验的主要步骤是________、________、滴定.
(4)工业上用电解法制备金属钠,但制备金属钾一般不采用电解熔融氯化钾,而是采用热还原法来制备.在850℃用金属钠来还原KCl反应如下:
Na(液)+KCl(液)![]() NaCl(液)+K(气).
NaCl(液)+K(气).
工业上应采用哪些措施才能使反应向正反应方向移动?
________.
解析:
答案:(1)日照时间长,水分蒸发快
(2)NaCl+CO2+H2O+NH3 NaHCO3↓+NH4Cl,2NaHCO3
NaHCO3↓+NH4Cl,2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
通过测定U形管反应前后的质量变化,求出反应产生CO2的量,进而计算出试样中的纯碱的质量分数
(3)称量 溶解
(4)不断分离出钾蒸气并冷凝
解析:(1)从盐田获得食盐需日照时间足够长,使大量水分蒸发.
(2)以NaCl为主要原料来制取纯碱,还需CO2与NH3,反应原理为:
NaCl+NH3+CO2+H2O NaHCO3↓+NH4Cl,2NaHCO3
NaHCO3↓+NH4Cl,2NaHCO3 Na2CO3+CO2↑+H2O.
Na2CO3+CO2↑+H2O.
而要测纯碱中
Na2CO3的含量,据装置可知通过Na2CO3与足量稀H2SO4反应生成CO2,测出CO2的质量,据原子守恒即可计算出Na2CO3的质量,继而求出其质量分数.(3)在中和滴定实验中主要实验步骤为称量、溶解、滴定.
(4)利用平衡移动的原理可知,不断将生成的钾蒸气分离出并冷凝,可促进平衡向正反应方向移动.


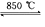 NaCl(l)+ K(g)。工业上应采用哪些措施才能使反应向正反应方向移动?___________________
NaCl(l)+ K(g)。工业上应采用哪些措施才能使反应向正反应方向移动?___________________