题目内容
6.下列溶质的溶液中C(H+)相同,则物质的量浓度最大的是( )| A. | HCl | B. | CH3COOH | C. | HClO4 | D. | H2SO4 |
分析 强电解质在溶液中完全电离,弱电解质在溶液中部分电离,氯化氢、高氯酸、硫酸都是强电解质,醋酸为弱电解质,则氢离子浓度相同时,醋酸的浓度最大.
解答 解:HCl、HClO4、H2SO4都是强酸,在溶液中完全电离,则c(HCl)=c(HClO4)=c(H+),c(H2SO4)=$\frac{1}{2}$c(H+),
CH3COOH为弱酸,在溶液中只能部分电离出氢离子,则c(CH3COOH)>c(H+),
所以物质的量浓度最大的是CH3COOH,
故选B.
点评 本题考查了弱电解质的电离,题目难度中等,明确强弱电解质的电离特点为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
16. 目前,我国有不法商贩用地沟油牟取暴利.医学研究证明,地沟油中的黄曲霉素强烈致癌.已知一种黄曲霉素的结构简式如图所示,关于该分子的说法中正确的是
目前,我国有不法商贩用地沟油牟取暴利.医学研究证明,地沟油中的黄曲霉素强烈致癌.已知一种黄曲霉素的结构简式如图所示,关于该分子的说法中正确的是
( )
 目前,我国有不法商贩用地沟油牟取暴利.医学研究证明,地沟油中的黄曲霉素强烈致癌.已知一种黄曲霉素的结构简式如图所示,关于该分子的说法中正确的是
目前,我国有不法商贩用地沟油牟取暴利.医学研究证明,地沟油中的黄曲霉素强烈致癌.已知一种黄曲霉素的结构简式如图所示,关于该分子的说法中正确的是( )
| A. | 1个分子中共含有30个δ键 | B. | 有5个碳原子采用sp3杂化 | ||
| C. | 属于极性分子,易溶于水 | D. | 分子中所有原子都在同一平面上 |
17.某同学学完《化学1》的知识后得出下列结论,其中正确的是( )
| A. | 将NaH溶于水,得到的水溶液能导电,由此可说明NaH是离子化合物 | |
| B. | Fe(OH)3胶体和Fe(OH)3沉淀的物理性质不同但化学性质基本相同 | |
| C. | CO2、SO2、SiO2、NO2等都是酸性氧化物;Na2O、MgO、A2lO3等都是碱性氧化物 | |
| D. | MnO2具有较强氧化性,可作为H2O2分解反应的氧化剂 |
14.一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)?3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%.其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
| A. | 2mol C | |
| B. | 2mol A、1mol B和1mol He(不参加反应) | |
| C. | 1mol B和1mol C | |
| D. | 2mol A、3mol B和3mol C |
1.将5.6g铁粉投入足量的100mL 2mol•L-1稀硫酸中,2min时铁刚好完全溶解.下列有关这个反应的速率表示正确的是( )
| A. | 铁的反应速率为0.5 mol•L-1•min-1 | |
| B. | 硫酸的反应速率为0.5 mol•L-1•min-1 | |
| C. | 硫酸亚铁的反应速率为0.25 mol•L-1•min-1 | |
| D. | 氢气的反应速率为0.5 mol•L-1•min-1 |
11.对食物的酸、碱性判断正确的是( )
| A. | 西瓜是酸性食物 | B. | 猪肉是碱性食物 | C. | 奶油是酸性食物 | D. | 大米是碱性食物 |
18.对食物的酸、碱性判断正确的是( )
| A. | 西瓜是酸性食物 | B. | 猪肉、牛肉是碱性食物 | ||
| C. | 鱿鱼、奶油是酸性食物 | D. | 大米、面包是碱性食物 |
16.下列说法正确的是( )
| A. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | |
| B. | Na2SO3溶液中:c(H+)+c(HSO3-)+c(H2SO3)═c(OH-) | |
| C. | 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 | |
| D. | 向含有AgCl固体的溶液中加入适量水使AgCl溶解又达到平衡时,在该温度下AgCl的溶度积不变,其溶解度也不变 |
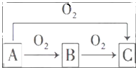 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):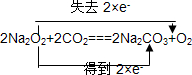 ,并用双线桥法表示上述反应中电子转移的方向和数目,如此反应转移0.5mol电子时,生成物中气体在标准状况下的体积为5.6L.如在AlCl3溶液中投入足量的(1)中的C物质,则反应的离子方程式为2Na2O2+Al3+═AlO2-+O2↑+4Na+.
,并用双线桥法表示上述反应中电子转移的方向和数目,如此反应转移0.5mol电子时,生成物中气体在标准状况下的体积为5.6L.如在AlCl3溶液中投入足量的(1)中的C物质,则反应的离子方程式为2Na2O2+Al3+═AlO2-+O2↑+4Na+.