题目内容
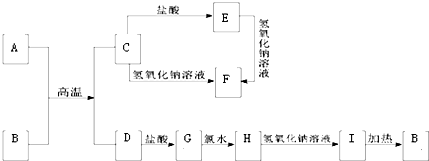
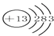
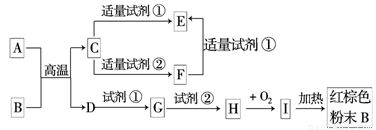
下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其它为化合物,其中C为两性氧化物.试推断:(友情提示:金属Al可在高温下将一些金属从其氧化物中置换出来)
(1)写出物质的化学式:
A:
(2)写出下列反应的方程式:
C→F的离子反应方程式

(1)写出物质的化学式:
A:
Al
Al
B:Fe2O3
Fe2O3
C:Al2O3
Al2O3
(2)写出下列反应的方程式:
C→F的离子反应方程式
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
H→I的化学反应方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
,相应的实验现象为白色沉淀迅速变成灰绿色,最终变成红褐色
白色沉淀迅速变成灰绿色,最终变成红褐色
.D与过量的稀硝酸反应的离子反应方程式Fe+4H++NO3-=Fe3++NO↑+2H2O
Fe+4H++NO3-=Fe3++NO↑+2H2O
.分析:C为两性氧化物,应为Al2O3,红棕色粉末B为Fe2O3,则A与B的反应应为铝热反应,A为Al,D为Fe,可与酸反应生成Fe2+,进而与碱反应生成Fe(OH)2,则试剂①为酸,试剂②为碱,则I为Fe(OH)3,E为铝盐,F为偏铝酸盐,以此解答该题.
解答:解:C为两性氧化物,应为Al2O3,红棕色粉末B为Fe2O3,则A与B的反应应为铝热反应,A为Al,D为Fe,可与酸反应生成Fe2+,进而与碱反应生成Fe(OH)2,则试剂①为酸,试剂②为碱,则I为Fe(OH)3,E为铝盐,F为偏铝酸盐,
(1)由以上分析可知A为Al,B为Fe2O3,C为Al2O3,故答案为:Al;Fe2O3;Al2O3;
(2)C→F的反应为Al2O3+2OH-=2AlO2-+H2O,H→I的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,相应的实验现象为白色沉淀迅速变成灰绿色,最终变成红褐色,D与过量的稀硝酸反应的离子反应方程式Fe+4H++NO3-=Fe3++NO↑+2H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;4Fe(OH)2+O2+2H2O=4Fe(OH)3;白色沉淀迅速变成灰绿色,最终变成红褐色;Fe+4H++NO3-=Fe3++NO↑+2H2O.
(1)由以上分析可知A为Al,B为Fe2O3,C为Al2O3,故答案为:Al;Fe2O3;Al2O3;
(2)C→F的反应为Al2O3+2OH-=2AlO2-+H2O,H→I的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,相应的实验现象为白色沉淀迅速变成灰绿色,最终变成红褐色,D与过量的稀硝酸反应的离子反应方程式Fe+4H++NO3-=Fe3++NO↑+2H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;4Fe(OH)2+O2+2H2O=4Fe(OH)3;白色沉淀迅速变成灰绿色,最终变成红褐色;Fe+4H++NO3-=Fe3++NO↑+2H2O.
点评:本题考查无机物的推断,明确红棕色物质B为氧化铁及A+B→D+C为铝热反应是解答本题的关键,题目难度不大,注意试剂②不一定为NaOH.

练习册系列答案
相关题目
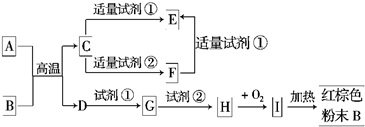 下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物.
下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物.