题目内容
研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入4mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
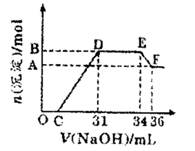
分析上述图形,下列说法不正确的是
- A.OC段离子反应方程式:H+十OH-=H2O
- B.溶液中结合OH-能力最强的离子是H+,最弱的离子是Al3+
- C.溶液中n(NH4+)=0.012mol
- D.欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量
B
试题分析:根据题意,没有气体放出,故还原产物为铵根离子,溶液中存在的离子为Al3+、Fe3+、H+、NH4+,根据谁碱性弱,谁结合氢氧根离子的能力就强,故与NaOH反应的先后顺序为H+、Fe3+、Al3+、NH4+,然后Al(OH)3反应溶解。根据DE段消耗NaOH3mL,可以计算n(NH4+)=n(NaOH)=0.003L×4mol/L=0.012mol,正确。
考点:考查元素及化合物知识与基本概念、基本理论的结合。
试题分析:根据题意,没有气体放出,故还原产物为铵根离子,溶液中存在的离子为Al3+、Fe3+、H+、NH4+,根据谁碱性弱,谁结合氢氧根离子的能力就强,故与NaOH反应的先后顺序为H+、Fe3+、Al3+、NH4+,然后Al(OH)3反应溶解。根据DE段消耗NaOH3mL,可以计算n(NH4+)=n(NaOH)=0.003L×4mol/L=0.012mol,正确。
考点:考查元素及化合物知识与基本概念、基本理论的结合。

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
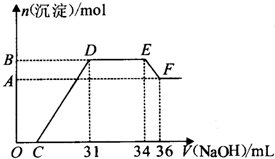 研究发现,硝酸越稀,还原产物中氮元素的化合价越低.某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出.在反应结束后的溶液中,逐滴加入5mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.下列说法正确的是( )
研究发现,硝酸越稀,还原产物中氮元素的化合价越低.某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出.在反应结束后的溶液中,逐滴加入5mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.下列说法正确的是( )| A、溶液中结合OH-能力最强的离子是NH4+ | B、D点时溶液中存在:c(NH4+)+c(H+)=c(OH-)+c(NO3-) | C、合金中n(Fe):n(Al)=1:3 | D、C的值为7 |
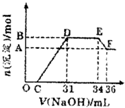 研究发现,硝酸越稀,还原产物中氮元素的化合价越低.某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出.在反应结束后的溶液中,逐滴加入4mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.分析上述图形,下列说法不正确的是( )
研究发现,硝酸越稀,还原产物中氮元素的化合价越低.某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出.在反应结束后的溶液中,逐滴加入4mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.分析上述图形,下列说法不正确的是( )| A、欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量 | B、溶液中结合OH-能力最强的离子是H+,最弱的离子是Al3+ | C、溶液中n(NH4+)=0.012mol | D、OC段离子反应方程式:H++OH-=H2O |

