题目内容
海洋是资源的宝库,海水中所含食盐高达4×1016t。用海水可生产食盐和金属
镁或镁的化合物,其过程如下图所示。
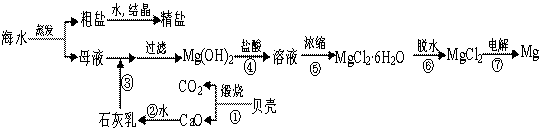 (1)贝壳主要成分的化学式 。
(1)贝壳主要成分的化学式 。
(2)步骤④反应的离子方程式 。
(3)实验室由粗盐结晶制精盐的操作包括溶解、过滤、蒸发等步骤。
A.粗盐提纯过程中过滤的目的是 (填序号)
①获得NaCl晶体 ②除去难溶性物质 ③除去易挥发物质 ④除去可溶性物质
B.过滤需要用到的玻璃仪器有玻璃棒 、 。
(4)Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物。某些材料因含有Mg(OH)2而具有阻燃性。简析Mg(OH)2能够阻燃的原因。
① ②
(5)电解MgCl2制金属Mg的反应方程式为:MgCl2![]() Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg g,同时可得到氯气 L(标准状况)。
Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg g,同时可得到氯气 L(标准状况)。
(1)CaCO3(1分) (2) Mg(OH)2+2H+=Mg2++2H2O (2分)
(3)A 、② (2分) B、漏斗、烧杯 (2分,每空1分)
(4)① Mg(OH)2受热分解生成MgO难熔物覆盖在可燃物表面阻止了可燃物的燃烧 (2分)
②分解生成的水会降低环境的温度。(2分) (5)4.8g (2分) 4.48L (2分)

 英才计划期末调研系列答案
英才计划期末调研系列答案
 109亿吨,故人类不存在缺水问题
109亿吨,故人类不存在缺水问题 (2)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。
(2)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。