题目内容
最近我国自主研制了一种新型燃料电池,一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.回答如下问题:
(1)以丁烷(C4H10)代表汽油,这个电池放电时发生反应的化学方程式是
(2)这个电池的正极发生的反应是
(3)用以上装置进行粗铜的精炼,提炼出1吨纯铜时,需要消耗燃料气(C4H10)
(4)请画出粗铜精炼的装置简图.(标出电极材料、电极名称、电解质溶液)

 .
.
(1)以丁烷(C4H10)代表汽油,这个电池放电时发生反应的化学方程式是
2C4H10+13O2→8CO2+10H2O
2C4H10+13O2→8CO2+10H2O
;(2)这个电池的正极发生的反应是
O2+4e-=2O2-
O2+4e-=2O2-
,固体电解质里O2-的移动方向是从正极移向负极
从正极移向负极
,向外电路释放电子的电极通入的是C4H10
C4H10
气体.(3)用以上装置进行粗铜的精炼,提炼出1吨纯铜时,需要消耗燃料气(C4H10)
27
27
m3 (在标准状况下).(计算结果取整数)(4)请画出粗铜精炼的装置简图.(标出电极材料、电极名称、电解质溶液)


分析:(1)根据燃料电池放电时发生反应是燃料燃烧的化学方程式来书写;
(2)该燃料电池的正极上是氧气发生得电子的还原反应,负极发生的是燃料丁烷失电子的氧化反应,电子从负极流向正极,据此来回答;
(3)进行粗铜的精炼时,需要消耗的燃料气可以根据装置中转移电子守恒知识来计算;
(4)粗铜精炼时,阳极材料是粗铜,阴极材料是精铜,电解质是含有铜离子的盐溶液.
(2)该燃料电池的正极上是氧气发生得电子的还原反应,负极发生的是燃料丁烷失电子的氧化反应,电子从负极流向正极,据此来回答;
(3)进行粗铜的精炼时,需要消耗的燃料气可以根据装置中转移电子守恒知识来计算;
(4)粗铜精炼时,阳极材料是粗铜,阴极材料是精铜,电解质是含有铜离子的盐溶液.
解答:解:(1)丁烷燃料电池放电时发生反应是丁烷燃烧的化学方程式,即2C4H10+13O2═8CO2+10H2O,
故答案为:2C4H10+13O2═8CO2+10H2O
(2)电池放电时负极发生的是燃料丁烷失电子的氧化反应,正极上是氧气发生的电子的还原反应,即:O2+4e-═2O2-,在燃料电池中,电解质里的阳离子移向正极,阴离子移向负极,所以电解质里O2-向负极移动,负极向外电路释放电子,
故答案为:O2+4e-═2O2-;从正极移向负极;C4H10;
(3)电解精炼铜时,在阴极上发生的电极反应是Cu2++2e-═Cu,当生成1吨金属时,转移电子的物质的量是:
=3.125×104mol,
根据电池反应:2C4H10+13O2═8CO2+10H2O,当转移这些电子时,需要消耗燃料气(C4H10)的体积是
×22.4L/mol≈27m3,
故答案为:27;
(4)粗铜精炼时,阳极材料是粗铜,阴极材料是精铜,电解质是含有铜离子的盐溶液,装置图为 ,
,
故答案为: .
.
故答案为:2C4H10+13O2═8CO2+10H2O
(2)电池放电时负极发生的是燃料丁烷失电子的氧化反应,正极上是氧气发生的电子的还原反应,即:O2+4e-═2O2-,在燃料电池中,电解质里的阳离子移向正极,阴离子移向负极,所以电解质里O2-向负极移动,负极向外电路释放电子,
故答案为:O2+4e-═2O2-;从正极移向负极;C4H10;
(3)电解精炼铜时,在阴极上发生的电极反应是Cu2++2e-═Cu,当生成1吨金属时,转移电子的物质的量是:
| 2×106g |
| 64g/mol |
根据电池反应:2C4H10+13O2═8CO2+10H2O,当转移这些电子时,需要消耗燃料气(C4H10)的体积是
| 3.125×104mol×2 |
| 52 |
故答案为:27;
(4)粗铜精炼时,阳极材料是粗铜,阴极材料是精铜,电解质是含有铜离子的盐溶液,装置图为
 ,
,故答案为:
 .
.点评:本题考查学生燃料电池以及电解精炼铜的工作原理知识,可以根据所学知识进行回答,注意电子守恒,难度不大.

练习册系列答案
相关题目
 ③CH3CH2CH3 ④HC
③CH3CH2CH3 ④HC CCH3
CCH3  ⑥CH3CH=CHCH3
⑥CH3CH=CHCH3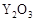 的
的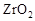 晶体,它在高温下能传导
晶体,它在高温下能传导 。回答如下问题:①以丁烷(
。回答如下问题:①以丁烷(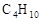 )代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。
)代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。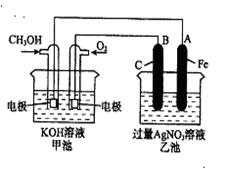
 ③CH3CH2CH3 ④HC
③CH3CH2CH3 ④HC CCH3
CCH3 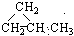 ⑥CH3CH=CHCH3
⑥CH3CH=CHCH3 的
的 晶体,它在高温下能传导
晶体,它在高温下能传导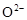 。回答如下问题:①以丁烷(
。回答如下问题:①以丁烷( )代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。
)代表汽油,这个电池放电时发生反应的化学方程式是_________________________________________________________。