题目内容
下列有关物质的性质与应用相对应的是
| A.氢氟酸具有酸性,可用于雕刻玻璃 |
| B.Na2O2具有强氧化性,可用作呼吸面具的供氧剂 |
| C.氯化铁溶液能溶解氧化铜,可用于制作印刷电路板 |
| D.SO2具有漂白性,可使酸性高锰酸钾溶液褪色 |
C
解析试题分析: 氢氟酸能用于雕刻玻璃的原因是氢氟酸具有强腐蚀性,A项错;Na2O2作呼吸面具的供氧剂时,既是氧化剂也是还原剂,B项错;氯化铁水解生成H+,H+与氧化铜反应,所以可用于制作印刷电路板,C项正确;SO2使酸性高锰酸钾褪色,不是因为漂白性,而是发生了氧化还原反应,D项错。
考点:本题考查常见无机物的性质与用途。

练习册系列答案
相关题目
下列说法中,不正确的是
①建国60周年庆典晚会上,天安门广场燃放的焰火是某些金属元素魅力的展现
②酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面有一层致密的氧化膜
③为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤KI淀粉溶液中通入Cl2,溶液变蓝,说明Cl2能与淀粉发生显色反应
| A.③④⑤ | B.①③④ | C.①③④⑤ | D.①②③④ |
下列说法正确的是
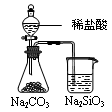
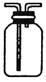
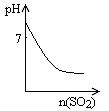
图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
| A.图I所示装置用于Cu和浓H2SO4制取少量的SO2气体 |
| B.图Ⅱ装置可验证非金属性:Cl>C>Si |
| C.图Ⅲ可用于收集气体H2、CO2、Cl2、NH3 |
| D.图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化 |
下列叙述正确的是
| A.将H2S通入FeCl3溶液中会产生淡黄色沉淀,继续通入则会产生黑色沉淀 |
| B.在中和热测定的实验中,将NaOH溶液和盐酸混合反应后的最高温度作为末温度 |
| C.分离Na2CO3溶液和CH3COOC2H5常用蒸馏法 |
| D.能使湿润的KI淀粉试纸变蓝的气体一定是Cl2 |
下表所列各组物质中,不能通过一步反应实现如图所示转化的是( )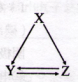
| 选项 | X | Y | Z |
| A | AlCl3 | Al(OH)3 | NaAlO2 |
| B | C | CO | CO2 |
| C | CH2=CH2 | CH3CH2Br | CH3CH2OH |
| D | S | SO2 | SO3 |
下列事实与结论(或推论)均正确的是
| A.将氨水加到盛有AgCl固体的试管中,AgCl固体完全溶解,说明所得溶液中c(Ag+)c(Cl-)>Ksp(AgCl) |
| B.物质的量之比为1: 2的Na2O2和NaHCO3的固体混合物,在密闭容器中充分加热反应后,残留的固体是Na2CO3 |
| C.向FeBr2溶液中通入少量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色;那么向FeI2溶液中通入少量的氯气,也会出现同样的现象 |
| D.将某混合气体通入品红溶液中,溶液不褪色,该气体中无Cl2 |
对下列实验装置叙述错误的是( )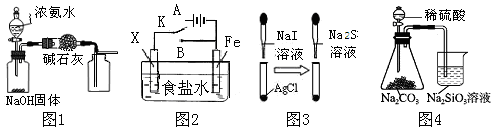
| A.图1:该装置不能制取并收集到干燥纯净的NH3 |
| B.图2:若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| C.图3:白色固体先变黄色,最后变成黑色,可以得出AgI溶解度小于Ag2S |
| D.图4:可以验证碳酸酸性强于硅酸 |
下列实验的现象及结论不正确的是
| A.过氧化钠放置在空气中,最终转变为白色粉末Na2CO3 |
| B.SO2通入BaCl2溶液中产生白色沉淀BaSO3 |
| C.打磨过的铝箔和未打磨的铝箔分别在空气中灼烧,两种铝箔均熔化但不滴落,说明氧化铝熔点比铝高 |
| D.分别向等物质的量浓度的Na2CO3和NaHCO3溶液中滴加酚酞,溶液都变红,Na2CO3溶液红色较深,说明Na2CO3水解程度大于NaHCO3 |
下列有关实验操作的叙述正确的是
| A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |
| C.NaCl溶液蒸发结晶时,蒸发皿中刚好有晶体析出时即停止加热 |
| D.向AlCl3溶液中滴加氨水,会产生白色沉淀,再加入NaHSO4溶液,沉淀不消失 |