题目内容
由Na、Na2O、Na2O2组成的固体混合物,其中各组分的物质的量之和为0.1mol,将其溶于水,所得溶液恰好能被150mL浓度为1mol/L的HCl溶液中和,下列相关描述说法不正确的是( )
分析:n(HCl)=0.15L×1mol/L=0.15mol,Na、Na2O、Na2O2组成的固体混合物溶于水反应都生成NaOH,根据NaOH+HCl=NaCl+H2O可知,n(NaOH)=n(HCl)=n(NaCl)=0.15mol,
设混合物中含有xmolNa,ymolNa2O,zmolNa2O2,则有
,
解之得x=0.05,y+z=0.05,根据反应2Na+2H2O=2NaOH+H2↑,Na2O+H2O=2NaOH,2Na2O2+2H2O=4NaOH+O2↑进行相关计算和判断.
设混合物中含有xmolNa,ymolNa2O,zmolNa2O2,则有
|
解之得x=0.05,y+z=0.05,根据反应2Na+2H2O=2NaOH+H2↑,Na2O+H2O=2NaOH,2Na2O2+2H2O=4NaOH+O2↑进行相关计算和判断.
解答:解:n(HCl)=0.15L×1mol/L=0.15mol,Na、Na2O、Na2O2组成的固体混合物溶于水反应都生成NaOH,根据NaOH+HCl=NaCl+H2O可知,n(NaOH)=n(HCl)=n(NaCl)=0.15mol,
设混合物中含有xmolNa,ymolNa2O,zmolNa2O2,则有
,
解之得x=0.05,y+z=0.05,
发生反应2Na+2H2O=2NaOH+H2↑,Na2O+H2O=2NaOH,2Na2O2+2H2O=4NaOH+O2↑,则
A.由以上分析可知,n(NaCl)=0.15mol,故A正确;
B.则2Na+2H2O=2NaOH+H2↑
0.05mol 0.025mol
2Na2O2+2H2O=4NaOH+O2↑
0.05mol 0.025mol
因是三种物质的混合物,由n(Na2O2)<0.05mol,则n(O2)<0.025mol,
所以H2和O2的体积比大于1:1,故B错误;
C.由x=0.05,y+z=0.05可知,x=y+z,Na、Na2O、Na2O2物质的量之比可能是2:1:1,因存在2=1+1,故C正确;
D.由x=0.05,y+z=0.05可知,x=y+z,Na、Na2O、Na2O2物质的量之比可能是5:3:2,因存在5=3+2,故D正确.
故选B.
设混合物中含有xmolNa,ymolNa2O,zmolNa2O2,则有
|
解之得x=0.05,y+z=0.05,
发生反应2Na+2H2O=2NaOH+H2↑,Na2O+H2O=2NaOH,2Na2O2+2H2O=4NaOH+O2↑,则
A.由以上分析可知,n(NaCl)=0.15mol,故A正确;
B.则2Na+2H2O=2NaOH+H2↑
0.05mol 0.025mol
2Na2O2+2H2O=4NaOH+O2↑
0.05mol 0.025mol
因是三种物质的混合物,由n(Na2O2)<0.05mol,则n(O2)<0.025mol,
所以H2和O2的体积比大于1:1,故B错误;
C.由x=0.05,y+z=0.05可知,x=y+z,Na、Na2O、Na2O2物质的量之比可能是2:1:1,因存在2=1+1,故C正确;
D.由x=0.05,y+z=0.05可知,x=y+z,Na、Na2O、Na2O2物质的量之比可能是5:3:2,因存在5=3+2,故D正确.
故选B.
点评:本题考查混合物的计算,题目难度较大,本题注意根据反应的方程式判断可能发生的反应,易错点为B,注意根据物质的量进行判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
以下是一些物质的熔沸点数据(常压):
|
|
钾 |
钠 |
Na2CO3 |
金刚石 |
石墨 |
|
熔点(℃) |
63.65 |
97.8 |
851 |
3550 |
3850 |
|
沸点(℃) |
774 |
882.9 |
1850(分解产生CO2) |
---- |
4250 |
金属钠和CO2在常压、890℃发生如下反应:
4 Na(g)+ 3CO2(g) 2
Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
2
Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
(1)上述反应的平衡常数表达式为 ;若4v正(Na)=3v逆(CO2),反应是否达到平衡 (选填“是”或“否”)。
(2)若反应在10L密闭容器、常压下进行,温度由890℃升高到1680℃,若反应时间为10min, 金属钠的物质的量减少了0.20mol,则10min里CO2的平均反应速率为 。
(3)高压下有利于金刚石的制备,理由是 。
(4)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
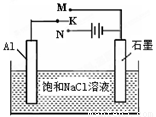
(5)下图开关K接M时,石墨作 极,电极反应式为 。K接N一段时间后测得有0.3mol电子转移,作出y随x变化的图象〖x—代表n(H2O)消耗,y—代表n[Al(OH)3],反应物足量,标明有关数据〗

无机化合物可根据其组成和性质进行分类:
(1)上述所示的物质分类方法名称是______.
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在表中.
(3)写出⑦转化为⑤的化学方程式:______.
(4)写出工业上由⑩制备O2的化学方程式:______ 2H2↑+O2↑,
(1)上述所示的物质分类方法名称是______.

(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在表中.
| 物质 类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②______ | ③______ ④Ba(OH)2 | ⑤Na2CO3 ⑥______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O |
(4)写出工业上由⑩制备O2的化学方程式:______ 2H2↑+O2↑,
