题目内容
6.X、Y、Z、W、R五种短周期元素在元素周期表中的位置如图所示,下列有关说法一定正确的是( )| X | Y | ||
| Z | W | R |
| A. | 非金属性的强弱顺序:Y>W>R | |
| B. | X、Y的气态氢化物的稳定性:X>Y | |
| C. | 原子半径的大小顺序:Z>W>Y | |
| D. | W、R的最高价氧化物对应水化物的酸性:W>R |
分析 A.若W为S、R为Cl时,Cl元素非金属性更强;
B.非金属性越强,氢化物越稳定;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大;
D.非金属性越强,最高价含氧酸的酸性越强.
解答 解:A.若W为S、R为Cl时,非金属性Cl>S,故A错误;
B.非金属性Y>X,非金属性越强,氢化物越稳定,故B错误;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径;Z>W>Y,故C正确;
D.若W为S、R为Cl时,非金属性Cl>S,非金属性越强,最高价含氧酸的酸性越强,故D错误,
故选:C.
点评 本题考查位置与性质关系,侧重考查元素周期律及元素周期表结构,需要学生熟练熟练掌握元素周期表.

练习册系列答案
相关题目
16. Na2CO3溶液中含碳元素微粒有多种,常温下,这些微粒的物质的量分数与溶液pH的变化关系如图所示.下列说法正确的是( )
Na2CO3溶液中含碳元素微粒有多种,常温下,这些微粒的物质的量分数与溶液pH的变化关系如图所示.下列说法正确的是( )
 Na2CO3溶液中含碳元素微粒有多种,常温下,这些微粒的物质的量分数与溶液pH的变化关系如图所示.下列说法正确的是( )
Na2CO3溶液中含碳元素微粒有多种,常温下,这些微粒的物质的量分数与溶液pH的变化关系如图所示.下列说法正确的是( )| A. | 在滴有酚酞的Na2CO3溶液中逐渐滴加盐酸至溶液恰好变为无色,得到NaHCO3溶液 | |
| B. | 有CO2气体放出的范围是pH≤5 | |
| C. | HCO3-的电离平衡常数为1×10-4 | |
| D. | pH=11的Na2CO3溶液稀释到体积为原来的100倍后pH=9 |
14.NA表示阿伏伽德罗常数.下列叙述中正确的是( )
| A. | 标准状况下,22.4LCCl4中含CCl4分子数为NA | |
| B. | 4.0gNaOH固体溶于100 mL水中,得到1 mol/L的NaOH溶液 | |
| C. | 常温常压,5.6gFe在足量Cl2中燃烧,转移的电子数为0.3NA | |
| D. | 分子总数为NA的SO2和CO2的混合气体中含有的氧原子数为4NA |
1.下列说法中,不正确的是( )
| A. | s区的元素都是活泼的金属元素 | B. | 所有的非金属元素都在p区 | ||
| C. | d区、ds区全是金属元素 | D. | 镧系、锕系元素都在f区 |
11.恒温下,将16mol N2与24mol H2的混合气体通入一个固定容积为4L的密闭容器中,发生如下反应:N2(g)+3H2(g)?2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是( )
| A. | 达到平衡时,N2和H2的转化率之比为1:1 | |
| B. | 10分钟内v(H2)=0.35mol/(L•min) | |
| C. | 平衡混合气体的密度为124g/L | |
| D. | 平衡混合气体中,n(N2):n(H2):n(NH3)=1:3:2 |
18. 1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如表:
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl,Na、Mg、Al第一电离能I1从小到大的排列顺序是Na<Al<Mg.
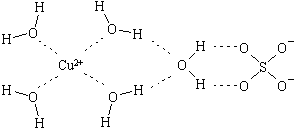
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.
①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是水分子间有氢键发生缔合作用.
②SO42-中S原子的杂化类型是sp3,与其互为等电子体的分子有CCl4(SiCl4)等(任写一种)
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有AC(填序号)
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式3d104s1;
金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是$\frac{4M}{{{N_A}{{(2\sqrt{2}r×{{10}^{-10}})}^3}}}$g/cm3(列出计算式).
 1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.
①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是水分子间有氢键发生缔合作用.
②SO42-中S原子的杂化类型是sp3,与其互为等电子体的分子有CCl4(SiCl4)等(任写一种)
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有AC(填序号)
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式3d104s1;
金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是$\frac{4M}{{{N_A}{{(2\sqrt{2}r×{{10}^{-10}})}^3}}}$g/cm3(列出计算式).
15.将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)?2G(g).忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如表所示:
①b<f ②915℃、2.0MPa时E的转化率为60%③该反应的△S>0 ④K(1000℃)<K(810℃)
上述①~④中正确的有( )
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
上述①~④中正确的有( )
| A. | ① | B. | ②④ | C. | ①②③ | D. | ①②③④ |
16.有甲、乙、丙、丁四种金属,仅甲在自然界主要以游离态存在;丙盐的水溶液不能用丁制的容器盛放;丁与乙盐的水溶液不反应.则这四种金属的活动性由强到弱的顺序可能是( )
| A. | 甲乙丙丁 | B. | 丁乙丙甲 | C. | 丙乙丁甲 | D. | 乙丁丙甲 |