题目内容
【题目】以铝土矿(主要成分为![]() )为原料冶炼金属铝,主要步骤包括:①将粉碎后的铝土矿溶解在氢氧化钠溶液中;②向①的所得溶液中通入过量二氧化碳,获得氢氧化铝固体;③使氢氧化铝脱水生成氧化铝;④……
)为原料冶炼金属铝,主要步骤包括:①将粉碎后的铝土矿溶解在氢氧化钠溶液中;②向①的所得溶液中通入过量二氧化碳,获得氢氧化铝固体;③使氢氧化铝脱水生成氧化铝;④……
(1)步骤④为冶炼金属铝的过程,应选择的方法是______(填序号)。
A.以C、![]() 或
或![]() 作还原剂 B.热分解法 C.利用铝热反应原理还原 D.电解法
作还原剂 B.热分解法 C.利用铝热反应原理还原 D.电解法
(2)步骤③所涉及反应的化学方程式为_____________________________________________。
(3)步骤①所涉及反应的离子方程式为_________________________________________________。
(4)步骤②至步骤③的过程中,须经过_____操作。
(5)步骤②所得溶液中含有的大量阴离子是________________(填离子符号)。
【答案】D ![]()
![]() 过滤
过滤 ![]()
【解析】
步骤①中,三氧化铝与氢氧化钠反应生成偏铝酸钠;步骤②中偏铝酸钠与二氧化碳反应生成氢氧化铝;步骤④采用电解法冶炼金属铝。
(1)工业上采用电解法冶炼金属铝,故答案选D。
(2)步骤③中氢氧化铝脱水生成氧化铝,化学反应方程式为: ![]() 。
。
(3)步骤①中![]() 与氢氧化钠反应生成偏铝酸钠,离子方程式为:
与氢氧化钠反应生成偏铝酸钠,离子方程式为:![]() 。
。
(4)步骤②反应产生氢氧化铝沉淀,故至步骤③的过程中要经过过滤操作。
(5)步骤②中通入过量的二氧化碳,二氧化碳与偏铝酸钠反应生成氢氧化铝和碳酸氢钠,故所得溶液中含有的大量阴离子为![]() 。
。

【题目】下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 用双氧水滴定KI-淀粉溶液 | 溶液变蓝 | 达到滴定终点 |
B | 向食用加碘盐中加入食醋和KI溶液,再加入CCl4振荡,静置 | 下层呈紫红色 | 该食用加碘盐中含有KIO3 |
C | 用湿润的淀粉碘化钾试纸鉴别NO2、溴蒸气 | 试纸变蓝 | 该气体为溴蒸气 |
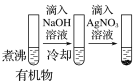
D |
| 最后试管有浅黄色沉淀 | 有机物中含有溴原子 |
A. AB. BC. CD. D