题目内容
把4.48LCO2通过一定量的固体过氧化钠后,收集到3.36L气体(标准状况),则3.36L气体质量是多少?
【答案】分析:根据通过差量法计算参加反应的二氧化碳体积、生成的氧气的体积,判断3.36L气体的组成及各成分的体积,再根据m=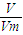 M计算各组分气体的物质质量并求和.
M计算各组分气体的物质质量并求和.
解答:解:令参加反应的CO2气体的体积为a,生成的O2的体积为b,则:
2CO2+2Na2O2=Na2CO3+O2 △V
2 1 1
a b 4.48L-3.36L=1.12L
解得:a=2.24L,b=1.12L,
因生成氧气的体积1.12L,小于3.36L,故二氧化碳有剩余,所以3.36L气体中CO2体积为4.48L-2.24L=2.24L,O2的体积为1.12L,
则4.48L气体的质量为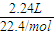 ×44g/mol+
×44g/mol+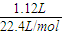 ×32g/mol=6.0g.
×32g/mol=6.0g.
答:3.36L气体质量是6.0g.
点评:本题考查差量法的运用,可以避免单独讨论或计算判断最后气体的组成,注意差量法的理解与运用,难度中等.
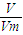 M计算各组分气体的物质质量并求和.
M计算各组分气体的物质质量并求和.解答:解:令参加反应的CO2气体的体积为a,生成的O2的体积为b,则:
2CO2+2Na2O2=Na2CO3+O2 △V
2 1 1
a b 4.48L-3.36L=1.12L
解得:a=2.24L,b=1.12L,
因生成氧气的体积1.12L,小于3.36L,故二氧化碳有剩余,所以3.36L气体中CO2体积为4.48L-2.24L=2.24L,O2的体积为1.12L,
则4.48L气体的质量为
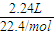 ×44g/mol+
×44g/mol+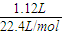 ×32g/mol=6.0g.
×32g/mol=6.0g.答:3.36L气体质量是6.0g.
点评:本题考查差量法的运用,可以避免单独讨论或计算判断最后气体的组成,注意差量法的理解与运用,难度中等.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目