题目内容
研究浓度对反应速率的影响时,我们采用同浓度同体积的酸性高锰酸钾溶液与不同浓度相同体积的草酸溶液反应,实验时发生的离子反应方程式是:
写出得出结论的实验现象是:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
写出得出结论的实验现象是:
加浓度大的草酸溶液时酸性高锰酸钾溶液褪色快
加浓度大的草酸溶液时酸性高锰酸钾溶液褪色快
.分析:酸性高锰酸钾溶液与草酸溶液反应生成硫酸锰、二氧化碳、硫酸钾和水;加浓度大的草酸溶液时酸性高锰酸钾溶液褪色快.
解答:解:酸性高锰酸钾溶液与草酸溶液反应生成硫酸锰、二氧化碳、硫酸钾和水,其反应离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;加入草酸溶液的浓度越大,反应越快,酸性高锰酸钾溶液褪色越快,
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;加浓度大的草酸溶液时酸性高锰酸钾溶液褪色快.
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;加浓度大的草酸溶液时酸性高锰酸钾溶液褪色快.
点评:本题考查了浓度对反应速率的影响,和离子方程式的书写,难度不大.

练习册系列答案
相关题目
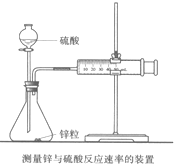 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究. 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.