题目内容
体积一定的绝热密闭容器中加入等物质的量的X、Y,进行如下可逆反应:X(g)+Y(g)?Z(g)+W(s)△H>0下列叙述正确的是( )
分析:A、通入X,X的浓度增大,使平衡向X浓度降低的方向移动;
B、继续充入Z,平衡逆向移动,Z的体积分数增大;
C、W是固体,移走部分W,不影响平衡;
D、反应热△H与化学计量数有关,与参加反应的反应物的物质的量无关.
B、继续充入Z,平衡逆向移动,Z的体积分数增大;
C、W是固体,移走部分W,不影响平衡;
D、反应热△H与化学计量数有关,与参加反应的反应物的物质的量无关.
解答:解:A、通入X,X的浓度增大,平衡向正反应方向移动,Y的转化率增大,故A正确;
B、继续充入Z,平衡逆向移动,Z的体积分数增大,故B错误;
C、W是固体,移走部分W,平衡不一定,故C错误;
D、反应热△H与化学计量数有关,化学计量数不变,反应热△H不变,与参加反应的反应物的物质的量无关,故D错误;
故选A.
B、继续充入Z,平衡逆向移动,Z的体积分数增大,故B错误;
C、W是固体,移走部分W,平衡不一定,故C错误;
D、反应热△H与化学计量数有关,化学计量数不变,反应热△H不变,与参加反应的反应物的物质的量无关,故D错误;
故选A.
点评:本题考查影响化学平衡的因素、热化学方程式的意义等,比较基础,注意D选项中反应热与参加反应的反应物的物质的量无关.

练习册系列答案
相关题目
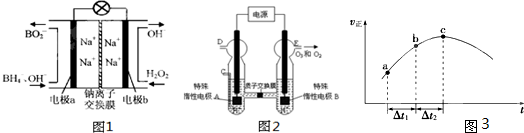
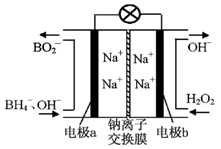
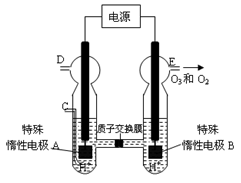
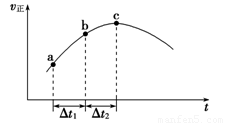
 (4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
(4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是 

 N2O4(g)达到平衡时NO2的体积分数
N2O4(g)达到平衡时NO2的体积分数 (NO2)随压强P的变化如图②所示,则A点的颜色深,B点的颜色浅
(NO2)随压强P的变化如图②所示,则A点的颜色深,B点的颜色浅 将增大
将增大
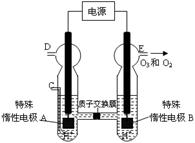
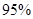 以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)
以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) 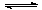 NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是 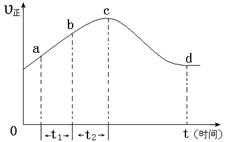
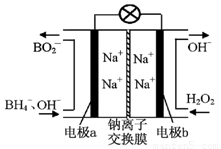
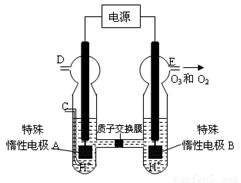
 (4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3
(g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
(4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3
(g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是