题目内容
2013年以来,全国很多地区都曾陷入严重的雾霾和污染天气中,冬季取暖排放的CO2、汽车尾气等都是形成雾霾的因素。
(1)已知:① N2(g) + O2(g)=2NO(g) △H=+179.5 kJ/mol
②2NO(g) + O2(g)=2NO2(g) △H=-112.3 kJ/mol
③2NO(g) +2CO(g)=N2(g) +2CO2(g) △H=-759.8 kJ/mol
下图是在101kPa,298K条件下1mol NO2和1mol CO反应生成1mol CO2和1mol NO过程中能量变化的示意图。则a= 。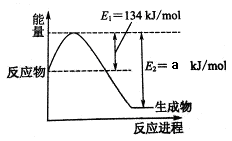
(2)将不同物质的量的H2O(g)和CO分别通入体积为2L的恒容密闭容器中,进行反应:
H2O(g)+CO(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO | H2 | |||
| 1 | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| 3 | 900 | a | b | c | d | t |
①实验组1中以v(CO2)表示的反应速率为 ,此温度下的平衡常数为 ,温度升高时平衡常数会 (填“增大”、“减小”或“不变”)。
②650℃时,若在此容器中开始充入2mol H2O(g)、 1mol CO、 1 mol CO2和 x molH2,若要使反应在开始时正向进行,则x应满足的条件是 。
③若a=2,b=1,则达平衡时实验组2中H2O(g)和实验组3中CO的转化率的关系为α2 (H2O) α3 (CO)(填“<”、“>”或“=”)。
(14分)(1)368(3分)(2)①0.16mol/(L·min) (2分) 8/3或2.67 (2分)减少 (2分) ②0≤x<16/3 (3分) ③ =(2分)
解析试题分析:(1)抑制① N2(g) + O2(g)=2NO(g) △H=+179.5 kJ/mol、②2NO(g) + O2(g)=2NO2(g) △H=-112.3 kJ/mol、③2NO(g) +2CO(g)=N2(g) +2CO2(g) △H=-759.8 kJ/mol,则根据盖斯定律可知(①-②+③)÷2即得到反应NO2(g)+CO(g)=NO(g) +CO2(g) △H=-234kJ/mol。则根据图像可知134kJ/mol-a kJ/mol=-234kJ/mol,解得a=368。
(2)①根据表中数据可知平衡时生成氢气的物质的量是1.6mol,则根据方程式可知消耗CO2的物质的量是1.6mol,其浓度是0.8mol/L,则CO2表示的反应速率为0.8mol/L÷5min=0.16mol/(L·min)。
② H2O(g)+CO(g) CO2(g)+H2(g)
CO2(g)+H2(g)
初始浓度 1mol/L 2mol/L 0 0
转化浓度 0.8mol/L 0.8mol/l 0.8mol/l 0.8mol/l
平衡浓度 0.2mol/L 1.2mol/L 0.8mol/l 0.8mol/l
所以平衡常数K=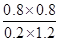 =2.67
=2.67
根据表中1、2数据可知,实验1中CO的转化率为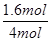 ×100%=40%,实验2中CO的转化率为
×100%=40%,实验2中CO的转化率为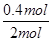 ×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,因此平衡常数减小;
×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,因此平衡常数减小;
②若要使反应在开始时正向进行,则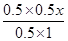 <2.67,解得x<16/3,因此x的取值范围是0≤x<16/3。
<2.67,解得x<16/3,因此x的取值范围是0≤x<16/3。
②实验2条件下平衡常数,需要列式计算平衡浓度
H2O(g)+CO(g) CO2(g)+H2(g)
CO2(g)+H2(g)
初始浓度 0.5mol/L 1mol/L 0 0
转化浓度 0.2mol/L 0.2mol/l 0.2mol/l 0.2mol/l
平衡浓度 0.3mol/L 0.8mol/L 0.2mol/l 0.2mol/l
则K=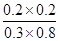 =0.17
=0.17
若a=2,b=1,则
H2O(g)+CO(g) CO2(g)+H2(g)
CO2(g)+H2(g)
初始浓度 1 0.5 0 0
转化浓度 x x x x
平衡浓度 1-x 0.5-x x x
则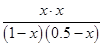 =0.17
=0.17
解得x=0.2
所以在这两种情况下实验组2中H2O(g)和实验组3中CO的转化率均是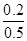 ×100%=40%。
×100%=40%。
考点:考查反应热、反应速率、平衡常数的有关计算与应用以及外界条件对平衡状态的影响

(14分)2013年12月2日,我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥三号”探月卫星成功送入太空,进一步向广寒宫探索。“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:①N2H4(g)+O2(g)=N2(g)+2H2O(g) △H = -543kJ·mol-1
②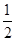 H2(g)+
H2(g)+ 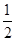 F2(g) = HF(g) △H = -269kJ·mol-1
F2(g) = HF(g) △H = -269kJ·mol-1
③H2(g)+ 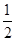 O2(g) = H2O(g) △H = -242kJ·mol-1
O2(g) = H2O(g) △H = -242kJ·mol-1
请写出肼和氟气反应的热化学方程式:_____________________________。
Ⅱ.氧化剂二氧化氮可由NO和 O2生成,已知在2 L密闭容器内,800 ℃时反应:
2NO(g)+O2(g) 2NO2(g) ΔH 的体系中,n(NO)随时间的变化如表:
2NO2(g) ΔH 的体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
| n(O2)(mol) | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(2)能说明该反应已达到平衡状态的是________。
A.容器内颜色保持不变 B. 2v逆(NO)=v正(O2)
C.容器内压强保持不变 D.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有 。
(4)在上述条件下,计算通入2 mol NO和1 mol O2的平衡常数K=______________。
(5)在上述条件下,若开始通入的是0.2 mol NO2气体,达到化学平衡时,则NO2的转化率为 。
(14分)(Ⅰ)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇。
已知某些化学键的键能数据如下表:
| 化学键 | C—C | C—H | H—H | C—O | C≡O | H—O |
| 键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
(1)已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为
;
(2)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(3)下列描述中能说明上述反应已达平衡的是 ;
A.2 v (H2)正=" v" (CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成 n molCO 的同时生成 2n molH2
(Ⅱ)回答下列问题:
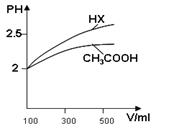
(1)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,
则Ka(HX) ______ Ka(CH3COOH)(填>、<或=)
(2)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中C(CH3COO?)-c(Na+)=_________mol·L-1(填精确值)。
化学反应原理对于工业生产和科研有重要意义
I、下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
| 化学反应 | 平衡常数 | 温度 | |
| 973 K | 1173 K | ||
①Fe(s)+CO2(g) FeO(s)+CO(g) FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) FeO(s)+H2(g) FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
③CO(g) +H2O(g) CO2(g) +H2(g) CO2(g) +H2(g) | K3 | ? | ? |
请回答:
(1)反应①是 (填“吸热”或“放热”)反应。
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=__________(用K1、K2表示)。
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有 _____(填写字母序号)。
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(4)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时__________________; t8时__________________。
②若t4时降压, t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
II、(5)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料.已知该装置的阳极反应为:4OH--4e-=O2↑+2H2O,则阴极反应为 。
(6)某空间站能量转化系统的局部如图所示,其中的燃料电池采用KOH溶液作电解液。

如果某段时间内,氢氧储罐中共收集到33.6L气体(已折算成标准状况),则该段时间内水电解系统中转移电子的物质的量为 mol。
捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3 (l)+ H2O (l)+ CO2 (g) (NH4)2CO3 (aq) △H1
(NH4)2CO3 (aq) △H1
反应Ⅱ:NH3 (l)+ H2O (l)+ CO2 (g) NH4HCO3 (aq) △H2
NH4HCO3 (aq) △H2
反应Ⅲ:(NH4)2CO3 (aq) + H2O (l)+ CO2 (g) 2NH4HCO3 (aq) △H3
2NH4HCO3 (aq) △H3
请回答下列问题:
(1)△H1与△H2、△H3之间的关系是:△H3= 。
(2)为研究温度对(NH4)2CO3捕获CO2气体效率的影响,在温度为T1、T2、T3、T4、T5的条件下,将等体积等浓度的(NH4)2CO3溶液分别置于等体积的密闭容器中,并充入等量的CO2气体,经过相同时间测得容器中CO2气体的浓度,得趋势图(下图1)。则:
①△H3______0 (填“>”、“=”或“<”)。
②温度高于T3,不利于CO2的捕获,原因是 。
③反应Ⅲ在温度为K1时,溶液pH随时间变化的趋势曲线如下图2所示。当时间到达t1时,将该反应体系温度迅速上升到K2,并维持该温度。请在该图中画出t1时刻后溶液的pH变化趋势曲线。
|

(3)利用反应Ⅲ捕获CO2,在(NH4)2CO3初始浓度和体积确定的情况下,提高CO2吸收量的措施有(写出1个) 。
(4)下列物质中也可能作为CO2捕获剂的是 。
A.NH4Cl B.Na2CO3 C.HOCH2CH2OH D.HOCH2CH2NH2
 CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):
CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):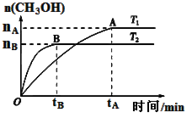
 2H2O + 。
2H2O + 。