题目内容
【题目】下列方程式不正确的是
A.NaHCO3在水中的电离方程式:NaHCO3 = Na++HCO![]()
B.氯化镁溶液与氨水反应的离子方程式:Mg2++2OH-= Mg(OH)2↓
C.Cl2与水反应的离子方程式:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
D.醋酸钠水解的离子方程式CH3COO-+H2O![]() CH3COOH+OH-
CH3COOH+OH-
【答案】B
【解析】
A.NaHCO3为强碱弱酸的酸式盐,属于强电解质,完全电离,但碳酸氢根离子属于弱酸根离子,不能拆,故电离方程式为NaHCO3= Na++HCO![]() ,A正确;
,A正确;
B.氨水中的溶质一水合氨为弱碱不能拆分,故氯化镁与氨水反应的正确离子方程式Mg2++2NH3H2O= Mg(OH)2↓+2NH4+,B错误;
C.HClO为弱酸,不能拆,故Cl2与水反应的离子方程式:Cl2+H2O![]() H++Cl-+HClO,C正确;
H++Cl-+HClO,C正确;
D.醋酸钠为强碱弱酸盐,醋酸钠水解的离子方程式:CH3COO-+H2O![]() CH3COOH+OH-,D正确;
CH3COOH+OH-,D正确;
故答案选B。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案【题目】一定温度下,在2 L的恒容密闭容器中发生反应![]() 。反应过程中的部分数据如下表所示:
。反应过程中的部分数据如下表所示:
n/mol t/min |
|
|
|
0 | 2.0 | 2.4 | 0 |
5 | 0.9 | ||
10 | 1.6 | ||
15 | 1.6 |
下列说法正确的是( )
A.0~5 min用A表示的平均反应速率为![]()
B.该反应在10 min后才达到平衡
C.平衡状态时,![]()
D.物质B的平衡转化率为20%
【题目】下表是A、B、C、D四种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色;②比例模型为 |
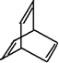
B | ①由C、H两种元素组成;②球棍模型为 |
C | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与D反应生成相对分子质量为100的酯 |
D | ①由C、H、O三种元素组成;②球棍模型为 |
回答下列问题:
(1)写出A与溴的四氯化碳溶液反应的化学方程式__________
(2)A与氢气发生加成反应后生成物质E,与E在分子组成和结构上相似的有机物有一大类(俗称"同系物"),它们均符合通式CnH2n+2。当n=______时,这类有机物开始出现同分异构体。
(3)B具有的性质是__________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式__________
(4)C与D反应能生成相对分子质量为100的酯,该反应的反应类型为____;其化学方程式为__________