题目内容
2.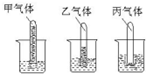 把分别盛有甲、乙、丙气体的试管到插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )
把分别盛有甲、乙、丙气体的试管到插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )| A. | 甲、乙、丙气体都易溶于水 | B. | 乙气体比甲气体更易溶于水 | ||
| C. | 可以采用排水集气方法收集丙气体 | D. | 不可以用排空气法收集甲气体 |
分析 由图可知,水进入试管说明气体溶于水,则丙气体不溶于水,甲、乙气体均可溶于水,且甲的溶解性较大,以此来解答.
解答 解:A.丙气体不溶于水,故A错误;
B.甲中试管水上升的高度大,则甲的溶解性较大,甲更易溶于水,故B错误;
C.丙气体不溶于水,则可以采用排水集气方法收集丙气体,故C正确;
D.不能确定甲气体的密度及能否与氧气反应等,哟该实验只能说明不能利用排水法收集甲,不能判断能否利用排空气法收集,故D错误;
故选C.
点评 本题考查实验装置的综合应用,为高频考点,把握实验装置的作用、物质的溶解性、气体收集方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
6.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,14g C2H4、C3H6的混合气体中含有碳原子的数目为NA | |
| B. | 常温下,pH=12的Na2CO3溶液中含有的OH-离子数为0.01NA | |
| C. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.2 NA | |
| D. | 含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
14.下列选项正确的是( )
| A. | 使PH试纸变成红色的溶液,可能存在大量的:NH4+、Cu2+、ClO-、Cl- | |
| B. | (NH4)2Fe(SO4)2溶液中,可能存在大量的:K+、Cu2+、Cl-、MnO4- | |
| C. | 硫酸酸化的淀粉KI溶液在空气中变成蓝色:4I-+O2+2H2O═2I2+4OH- | |
| D. | NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
12.在高科技工业上,有的高分子材料能用在能量的转换上.如传感膜能把化学能转化为电能,热电膜能把热能转化为电能等,这种高分子材料是( )
| A. | 高分子膜 | B. | 医用高分子材料 | C. | 生物高分子材料 | D. | 液晶高分子材料 |