题目内容
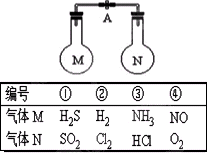
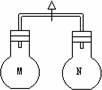
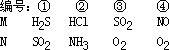
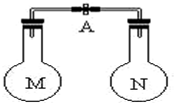 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( ) 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
|
分析:相同温度下,一定体积的容器中气体压强与气体的物质的量成之比,气体的物质的量越大其压强越大,据此分析解答.
解答:解:①氯气和碘化氢反应生成氯化氢和碘单质,即Cl2+2HI═2HCl+I2.碘单质常温下是固体,反应后气体体积减小为原来体积的
;
②氨气和氯化氢反应生成氯化铵固体,反应后气体压强为零;
③氢气和氮气在常温下不反应,气压不变;
④一氧化氮和氧气化合会生成二氧化氮,即2NO+O2═2NO2,然后发生2NO2?N2O4,反应后气体体积减小,要比原来体积的
还要小;
所以最后容器内的压强由大到小的顺序为③>①>④>②,
故选:B.
| 2 |
| 3 |
②氨气和氯化氢反应生成氯化铵固体,反应后气体压强为零;
③氢气和氮气在常温下不反应,气压不变;
④一氧化氮和氧气化合会生成二氧化氮,即2NO+O2═2NO2,然后发生2NO2?N2O4,反应后气体体积减小,要比原来体积的
| 2 |
| 3 |
所以最后容器内的压强由大到小的顺序为③>①>④>②,
故选:B.
点评:本题考查物质间的反应,明确物质的性质并根据差量法来分析解答,④中易漏掉二氧化氮和四氧化二氮之间的转化而导致错误,为易错点.

练习册系列答案
相关题目
|
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是
| |
| [ ] | |
A. |
①②③④ |
B. |
②④①③ |
C. |
④①②③ |
D. |
①④③② |
|
室温时,两个容积相同的烧瓶中分别盛满M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),最后容器内的压强由大到小的顺序是
| |
| [ ] | |
A. |
①②③④ |
B. |
②④①③ |
C. |
④①②③ |
D. |
①④③② |