题目内容
某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是
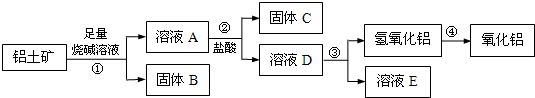
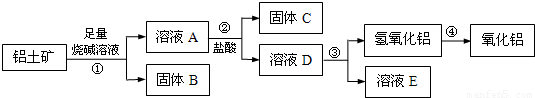
Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:

(1)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是
;
;
第③步中,生成氢氧化铝的离子方程式是
。
(2)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是________。(保留一位小数)
(3)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol 碳单质,转移1mol电子,反应的化学方程式是 。
(1) Al2O3+2OH-= 2AlO2-+H2O (2分) SiO2+2OH-= SiO32-+ H2O (2分)
Al3+ +3NH3·H2O=Al(OH)3↓+ 3NH4+(写AlCl3与NaOH的反应不给分)(2分)
(2)65.4% (2分) (3)Al2O3+3Cl2+3C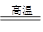 2AlCl3 +3CO (2分)
2AlCl3 +3CO (2分)
【解析】
试题分析:(1)氧化铁和氢氧化钠溶液不反应,氧化铝和二氧化硅能和氢氧化钠溶液反应,则向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是Al2O3+2OH-= 2AlO2-+H2O、SiO2+2OH-= SiO32-+ H2O。固体B是氧化铁,A中含有偏铝酸钠和硅酸钠以及过量的氢氧化钠,则加入过量的盐酸后生成硅酸沉淀和氯化铝,即固体C是硅酸,D中含有氯化铝和盐酸,因此反应③中生成氢氧化铝的试剂是氨气或氨水,则生成氢氧化铝的离子方程式是Al3++3NH3·H2O=Al(OH)3↓+ 3NH4+。
(2)所得氢氧化铝固体的质量与原铝土矿质量相等,这说明铝土矿中Al2O3的质量分数和氢氧化铝中氧化铝的质量分数是相同的。又因为氧化铝可以写成Al2O3·3H2O的形式,所以质量分数是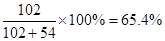 。
。
(3)每消耗0.5 mol 碳单质,转移1mol电子,这说明反应中碳失去2个电子,即氧化产物是CO,所以反应的化学方程式是Al2O3+3Cl2+3C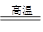 2AlCl3 +3CO。
2AlCl3 +3CO。
考点:考查物质的分离与提纯、方程式的书写以及物质含量的有关计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生答题能力的培养,有利于培养学生的逻辑推理能力和发散思维能力,也有利于培养学生的规范答题能力和应试能力。

 名校课堂系列答案
名校课堂系列答案