题目内容
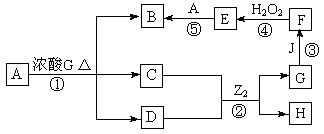
.(12分)在下图转化关系中,固体甲的焰色反应呈黄色,M为常见的液体物质,I为常见金属,且I与G的稀溶液不反应,只能与G的浓溶液在加热条件下反应;酸G是重要的化工产品和化工原料;H为良好的耐火材料(图中部分产物没有列出)。

(1)固体甲的名称为__________,F的化学式为______________。
(2)反应①~⑦中属于氧化还原反应的是______________(填写反应序号)。
(3)工业废气中常含有气体E,为了充分利用资源、保护环境,目前应用最广泛的工业废气处理方法是石灰法。以生石灰为原料在吸收装置中与气体E反应的化学方程式为:
___________________________________________。
(4)反应⑦的化学反应方程式为_____________________________________________。
(5)已知工业上电解熔融的H冶炼金属单质X,向40.0g固体混合物中(仅含H、Fe2O3、SiO2),加入足量稀盐酸,分离得到12.0g固体;滤液中加入过量A溶液,分离得到21.4g固体;则此混合物中元素X的质量分数为__________________。

(1)固体甲的名称为__________,F的化学式为______________。
(2)反应①~⑦中属于氧化还原反应的是______________(填写反应序号)。
(3)工业废气中常含有气体E,为了充分利用资源、保护环境,目前应用最广泛的工业废气处理方法是石灰法。以生石灰为原料在吸收装置中与气体E反应的化学方程式为:
___________________________________________。
(4)反应⑦的化学反应方程式为_____________________________________________。
(5)已知工业上电解熔融的H冶炼金属单质X,向40.0g固体混合物中(仅含H、Fe2O3、SiO2),加入足量稀盐酸,分离得到12.0g固体;滤液中加入过量A溶液,分离得到21.4g固体;则此混合物中元素X的质量分数为__________________。

本题为元素及化合物的推断题,在解题中要充分分析题目所给的信息,找出突破口。(1)固体甲为焰色为黄色,故为钠及其化合物;(2)M为液体,在中学的物质中溶液很多,但液体不多,可以推测为水、硫酸等;(3)气体C气体E气体F,这个过程可能为连续氧化,推测可能为S、N等,又因为金属I与酸G,在加热的条件下反应,不是HNO3,而应该为H2SO4,从而确定C为H2S;(4)固体乙与M的反应为水解反应,故乙为金属硫化物,又从H为防火材料,电解熔融物得到金属单质,可确定为Al。

练习册系列答案
相关题目





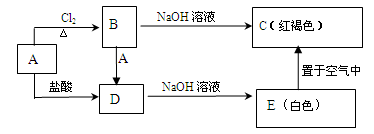
 示)
示) (用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
(用元素符号表示),下列表述中能证明这一事实的是 (填序号)。