题目内容
【题目】把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58 g白色难溶物析出,向所得溶液中逐滴加人0.5 mol L-1的盐酸,加入盐酸的体积和生成沉淀的质量如下图所示:
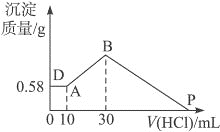
请计算:
(1)混合物中A1C13和MgCl2的质量____________________;
(2)P点表示盐酸加入的体积____________________。
【答案】AlCl3:1.335g MgCl2:0.95g130mL
【解析】
(1)由图可知,加入盐酸,开始沉淀的量不变,后来才有沉淀增加,说明NaOH在与AlCl3全部反应生成NaAlO2后还有剩余,则可判断0.58 g沉淀为Mg(OH)2,物质的量为0.01 mol,所以原MgCl2也是0.01 mol,质量为0.95 g。图中AB段发生的反应是:NaAlO2+HCl+H2O =Al(OH)3↓+NaCl,由方程式可得:n(HCl)=n[Al(OH)3]=n(Al)=0.5 mol/L×(0.03-0.01)L=0.01 mol,原AlCl3的质量为0.01 mol×133.5 g/mol=1.335 g;(2)混合物中NaOH的物质的量是剩余的NaOH和AlCl3、MgCl2消耗的NaOH物质的量的总和n(NaOH)=0.5 mol/L×0.01 L+0.01 mol×4+0.01 mol×2=0.065 mol,P点时消耗的盐酸等于原NaOH的物质的量0.065 mol,此时盐酸的体积是V=![]() =0.13 L=130 mL。
=0.13 L=130 mL。

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目