题目内容
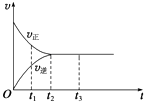
【题目】在100mLNaOH溶液中加入NH4NO3 和(NH4)2SO4 的固体混合物,加热使之充分反应,如图表示加入固体的质量与产生气体的体积(标准状况)的关系.试计算: 
(1)NaOH溶液的物质的量浓度是molL﹣1
(2)当NaOH溶液为140mL,固体为51.6g时,充分反应产生的气体为L(标准状况)
(3)当NaOH溶液为180mL,固体仍为51.6g时,充分反应产生的气体为L(标准状况).
【答案】
(1)5
(2)15.68
(3)16.8
【解析】解:(1)氢氧化钠与NH4NO3和(NH4)2SO4的混合物生成氨气,发生反应NH4++OH﹣ ![]() NH3↑+2H2O,从图中可看出34.4 g混合物和100 mL NaOH恰好完全反应.则n(NaOH)=n(NH3)=
NH3↑+2H2O,从图中可看出34.4 g混合物和100 mL NaOH恰好完全反应.则n(NaOH)=n(NH3)= ![]() =0.5 mol,c(NaOH)=
=0.5 mol,c(NaOH)= ![]() =5mol/L,所以答案是:5;(2)当固体混合物的质量是51.6 g时,固体混合物完全反应消耗的氢氧化钠溶液的体积为
=5mol/L,所以答案是:5;(2)当固体混合物的质量是51.6 g时,固体混合物完全反应消耗的氢氧化钠溶液的体积为 ![]() ×100mL=150mL,而V(NaOH)=140 mL,说明固体过量,所以n(NH3)=n(NaOH)=5 mol/L×0.14 L=0.7mol,V(NH3)=0.7mol×22.4 L/mol=15.68 L,所以答案是:15.68;(3)由(2)分析可知,当V(NaOH)=180 mL时,说明NaOH过量,则固体51.6 g完全反应,故V(NH3)=11.2L×
×100mL=150mL,而V(NaOH)=140 mL,说明固体过量,所以n(NH3)=n(NaOH)=5 mol/L×0.14 L=0.7mol,V(NH3)=0.7mol×22.4 L/mol=15.68 L,所以答案是:15.68;(3)由(2)分析可知,当V(NaOH)=180 mL时,说明NaOH过量,则固体51.6 g完全反应,故V(NH3)=11.2L× ![]() =16.8 L, 所以答案是:16.8.
=16.8 L, 所以答案是:16.8.

【题目】下列关于电解质的判断中,正确的观点是( )
A. 在熔融状态下能导电的物质
B. 在水溶液或熔融状态下能导电的物质
C. 在水溶液或熔融状态下能导电的化合物
D. 在水溶液和熔融状态下都能导电的化合物
【题目】下列分离和提纯的实验中,所选用的方法或仪器不正确的是( )
序号 | A | B | C | D |
实验目的 | 制取蒸馏水 | 分离水和植物油 | 分离食盐水与泥沙 | 从浓食盐水中得到氯化钠晶体 |
分离方法 | 蒸馏 | 分液 | 萃取 | 蒸发 |
选用仪器 |
|
|
|
|
A.选项A
B.选项B
C.选项C
D.选项D
【题目】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外电子数之和为21.下列关系正确的是( )
W | X | |||
Y | Z |
A. 氢化物沸点:W<Z
B. 氧化物对应水化物的酸性:Y>W
C. Y2X3与YZ3化合物类型相同
D. 简单离子的半径:Y<X
【题目】下图是元素周期表的一部分,表中的①~⑨中元素,用元素符号或化学式填空回答:
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为___________。
(2)地壳中含量最多的金属元素是____________________________。
(3)②与④形成的化合物的电子式______________________________。
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是___________,碱性最强的是____________,呈两性的氢氧化物是__________________。