题目内容
能够证明SO2中含有CO2的方法是( )
| A、通入澄清石灰水 |
| B、通入品红溶液 |
| C、先通入酸性KMnO4溶液,再依次通入品红溶液、澄清石灰水 |
| D、先通入饱和NaHCO3溶液,再依次通入品红溶液、澄清石灰水 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:证明SO2中含有CO2的,先利用二氧化硫的还原性除去二氧化硫,再利用石灰水检验二氧化碳,注意二者均能使石灰水变浑浊,以此来解答.
解答:
解:A.二者均能使石灰水变浑浊,不能鉴别,故A不选;
B.品红可鉴别二氧化硫,故B不选;
C.先通入酸性KMnO4溶液除去二氧化硫,再依次通入品红溶液说明不存在二氧化硫,最后利用澄清石灰水验证二氧化碳的存在,故C选;
D.先通入饱和NaHCO3溶液,与二氧化硫反应生成二氧化碳,干扰原混合气体中二氧化碳的检验,故D不选;
故选C.
B.品红可鉴别二氧化硫,故B不选;
C.先通入酸性KMnO4溶液除去二氧化硫,再依次通入品红溶液说明不存在二氧化硫,最后利用澄清石灰水验证二氧化碳的存在,故C选;
D.先通入饱和NaHCO3溶液,与二氧化硫反应生成二氧化碳,干扰原混合气体中二氧化碳的检验,故D不选;
故选C.
点评:本题考查物质的鉴别,为高频考点,把握物质的性质及性质差异为解答的关键,注意现象相同不能鉴别物质,综合考查元素化合物知识,选项D为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将固体NH4I置于密闭容器中,在某温度下,发生下列反应:
NH4I(s)?NH3(g)+HI(g);2HI(g)?H2(g)+I2(g)
当达化学平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则容器中NH3、HI、I2的物质的量之比是( )
NH4I(s)?NH3(g)+HI(g);2HI(g)?H2(g)+I2(g)
当达化学平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则容器中NH3、HI、I2的物质的量之比是( )
| A、8:8:1 |
| B、10:8:1 |
| C、2:2:1 |
| D、3:2:1 |
区别SO2和CO2气体可选用( )
| A、通入澄清石灰水中 |
| B、通入品红溶液中 |
| C、用带火星的木条检验 |
| D、通入石蕊试液中 |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )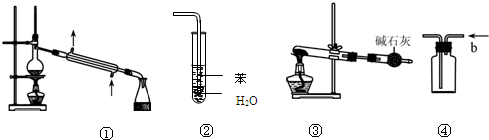

| A、装置①常用于分离互相溶沸点不同的液体混合物 |
| B、装置②可用于吸收HCl气体,并防止倒吸 |
| C、以NH4HCO3为原料,装置③可用于实验室制备少量NH3 |
| D、装置④b口进气可收集CO2、NO等气体 |
可逆反应 CO(g)+H2O(g)?CO2(g)+H2(g),温度为749K时,K=1;CO的起始浓度为2mol?L-1,H2O的起始浓度为6mol?L-1时,在密闭容器达到平衡,CO的转化率为( )
| A、80% | B、75% |
| C、50% | D、25% |
1992年,我国取得的重大科技成果之一是发现了三种元素的新的同位素,其中一种是
Hg,它的质子数与中子数相差( )
208 80 |
| A、80 | B、128 |
| C、208 | D、48 |
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )

| A、X是正极,Y是负极,CuSO4溶液的pH逐渐减小 |
| B、X是正极,Y是负极,CuSO4溶液的pH保持不变 |
| C、X是负极,Y是正极,CuSO4溶液的pH逐渐减小 |
| D、X是负极,Y是正极,CuSO4溶液的pH保持不变 |
某有机物分子中含有下列基团:2个 、2个-CH2-、3个-CH3和一个-COOH,该有机物可能的结构有(不考虑立体异构)( )
、2个-CH2-、3个-CH3和一个-COOH,该有机物可能的结构有(不考虑立体异构)( )
 、2个-CH2-、3个-CH3和一个-COOH,该有机物可能的结构有(不考虑立体异构)( )
、2个-CH2-、3个-CH3和一个-COOH,该有机物可能的结构有(不考虑立体异构)( )| A、8种 | B、9种 |
| C、10种 | D、11种 |
分类是化学学习与研究的常用方法,下列分类正确的是( )
| A、Na2O、MgO、Al2O3均属于碱性氧化物 |
| B、根据电解质在水溶液中电离的程度,将电解质分为强电解 质和弱电解质 |
| C、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D、石灰石、生石灰、熟石灰均属于碱 |