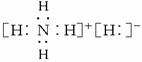题目内容
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外层电子层结构,则下列有关说法中,不正确的是( )
分析:NH5所有原子的最外层都符合相应稀有气体原子的最外层电子层结构,即氮原子最外层达到8电子稳定结构,所有氢原子达到2电子稳定结构,所以,NH5是离子化合物氢化铵,铵根中的氮原子与四个氢原子形成四个共价键,符合稀有气体原子的最外层结构,剩余的一个氢原子只能是H-,这样才符合2电子的稳定结构,所以数铵根离子和氢阴离子形成的离子化合物,能稳定存在于固体中类似氯化铵.
解答:解:A、根据氮原子的原子结构,最外层5个电子最多和四个氢原子形成共价键(其中一个是配位键,氮原子提供一对电子,氢离子提供空轨道形成),形成了带正电荷的铵根离子,所以另一个氢原子只能是形成H-,阴阳离子间形成离子键,故A错误;
B、由分析可知该化合物为NH4H,既存在离子键又存在共价键,故B正确;
C、根据离子化合物的结构特征,阳离子是铵根离子,阴离子是氢阴离子,都达到了稀有气体的最外层结构,电子式正确,故C正确;
D、与盐酸反应,NH4H+HCI=NH4CI+H2↑,是H-和H+间的氧化还原反应,故D正确;
故选A.
B、由分析可知该化合物为NH4H,既存在离子键又存在共价键,故B正确;
C、根据离子化合物的结构特征,阳离子是铵根离子,阴离子是氢阴离子,都达到了稀有气体的最外层结构,电子式正确,故C正确;
D、与盐酸反应,NH4H+HCI=NH4CI+H2↑,是H-和H+间的氧化还原反应,故D正确;
故选A.
点评:本题考查了原子间化学键的形成,原子最外层电子的稳定结构形成,电子式的书写.

练习册系列答案
相关题目