题目内容
物质的分类方法有:交叉分类法、树状分类法等多种方法,下列对无机化合物分类如图:
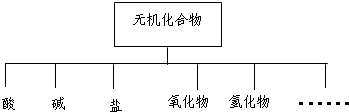
(1)如图所示的物质分类方法名称是______.
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②、④、⑥后面.
(3)写出⑦与过量的③溶液反应的离子方程式______.
(4)3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O反应中,氧化剂是______,氧化产物是______.若有3molCu完全反应,转移电子数为______mol.
(5)实验室制备⑨的化学方程式为______.

(1)如图所示的物质分类方法名称是______.
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②、④、⑥后面.
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HNO3 ②______ | ③NaOH ④______ | ⑤Na2SO4 ⑥______ | ⑦SO2 ⑧SO3 | ⑨NH3 |
(4)3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O反应中,氧化剂是______,氧化产物是______.若有3molCu完全反应,转移电子数为______mol.
(5)实验室制备⑨的化学方程式为______.
(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,有叶、枝、杆、根,图示方法就是树状图,故答案为:树状分类法;
(2)酸电离出的阳离子全部是氢离子的化合物,如H2SO4;碱电离出的阴离子全部为氢氧根离子,如NaOH;盐电离出得阳离子为金属离子,阴离子为酸根离子,如KNO3,
故答案为:②H2SO4;④NaOH;⑥KNO3;
(3)二氧化硫和氢氧化钠反应生成水和亚硫酸钠,其反应的离子方程式为:SO2+2OH-═SO32-+H2O,故答案为:SO2+2OH-═SO32-+H2O;
(4)3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O反应中,N元素的化合价降低,所以氧化剂是HNO3,铜元素化合价升高,是还原剂反应产物是氧化产物,所以氧化产物是 Cu(NO3)2;Cu从0价升高到+2价失去2个电子,所以若有3mol Cu完全反应,转移电子数为6mol,
故答案为:HNO3;Cu(NO3)2; 6;
(5)实验室用加热氢氧化钙和氯化铵固体混合物的方法来制取氨气,其反应的化学方程式为:Ca(OH)2+2NH4Cl
CaCl2+2H2O+2NH3↑,
故答案为:Ca(OH)2+2NH4Cl
CaCl2+2H2O+2NH3↑.
(2)酸电离出的阳离子全部是氢离子的化合物,如H2SO4;碱电离出的阴离子全部为氢氧根离子,如NaOH;盐电离出得阳离子为金属离子,阴离子为酸根离子,如KNO3,
故答案为:②H2SO4;④NaOH;⑥KNO3;
(3)二氧化硫和氢氧化钠反应生成水和亚硫酸钠,其反应的离子方程式为:SO2+2OH-═SO32-+H2O,故答案为:SO2+2OH-═SO32-+H2O;
(4)3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O反应中,N元素的化合价降低,所以氧化剂是HNO3,铜元素化合价升高,是还原剂反应产物是氧化产物,所以氧化产物是 Cu(NO3)2;Cu从0价升高到+2价失去2个电子,所以若有3mol Cu完全反应,转移电子数为6mol,
故答案为:HNO3;Cu(NO3)2; 6;
(5)实验室用加热氢氧化钙和氯化铵固体混合物的方法来制取氨气,其反应的化学方程式为:Ca(OH)2+2NH4Cl
| ||
故答案为:Ca(OH)2+2NH4Cl
| ||

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目


 m数量级的小颗粒制成的材料
m数量级的小颗粒制成的材料 m数量级的小颗粒制成的材料
m数量级的小颗粒制成的材料 m数量级的小颗粒制成的材料
m数量级的小颗粒制成的材料