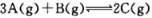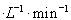题目内容
有A、B、C三种气体,若起始时取1mol A与2mol B,发生反应A+2B?2C.达到平衡时c(A)、c(B)、c(C)之比与反应速率vA、vB、vC之比恰好相同,则A的平衡转化率为( )
分析:到平衡时c(A)、c(B)、c(C)之比与反应速率vA、vB、vC之比恰好相同,即浓度之比等于物质的量之比等于化学方程式中的系数比相同,依据化学平衡三段式列式得计算,根据转化率概念计算得到;
解答:解:设反应达到平衡A的消耗物质的量为x,依据化学平衡三段式得到:
A+2B?2C
起始量(mol) 1 2 0
变化量(mol) x 2x x
平衡量(mol) 1-x 2-2x x
到平衡时c(A)、c(B)、c(C)之比与反应速率vA、vB、vC之比恰好相同,即浓度之比等于物质的量之比等于化学方程式中的系数比相同
(1-x):(2-2x):x=1:2:1;
计算得到x=0.5mol;
A的转化率=50%;
故选:C.
A+2B?2C
起始量(mol) 1 2 0
变化量(mol) x 2x x
平衡量(mol) 1-x 2-2x x
到平衡时c(A)、c(B)、c(C)之比与反应速率vA、vB、vC之比恰好相同,即浓度之比等于物质的量之比等于化学方程式中的系数比相同
(1-x):(2-2x):x=1:2:1;
计算得到x=0.5mol;
A的转化率=50%;
故选:C.
点评:本题考查了化学平衡的计算应用,注意平衡状态下物质的浓度之比等于物质的量之比,化学反应速率之比等于化学方程式的系数之比,题目难度中等.

练习册系列答案
相关题目