题目内容
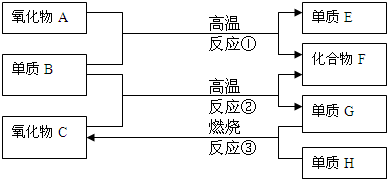
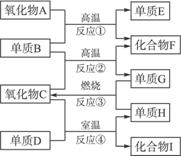
如下图,已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;
③化合物I能溶于水呈酸性,它能够跟氧化物A起反应。

据此,请填空:
(1)化合物F是____________。
(2)化合物I是____________。
(3)反应③的化学方程式是________________________________________________。
(4)反应④的化学方程式是________________________________________________。
解析:本题考查元素及其化合物的性质,属常规“方框图”题型。单质E和化合物F分别是半导体材料和不成盐氧化物,因而它们的首选答案可考虑各为Si和CO,于是,反应①的化学方程式应为:
SiO2+2C![]() Si+2CO↑
Si+2CO↑
氧化物A是SiO2,它除了跟氢氟酸反应外不跟任何酸起反应,由此判断化合物I为HF。需作进一步检验,此时要对所有参与反应的各种物质加以考虑。现试写出其余三个反应的化学方程式如下:
反应②为:C+H2O![]() CO+H2
CO+H2
反应③为:2H2+O2![]() 2H2O
2H2O
反应④为:![]() 4HF+O2
4HF+O2
经逐一核对,各物质均符合题意。显然,本题的“切入点”,可以认为是Si和CO,而HF和F2则是本题的难点和重点之所在。
答案:(1)CO(一氧化碳) (2)HF(氟化氢)
(3)2H2+O2![]() 2H2O
2H2O
(4)![]() 4HF+O2
4HF+O2

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目